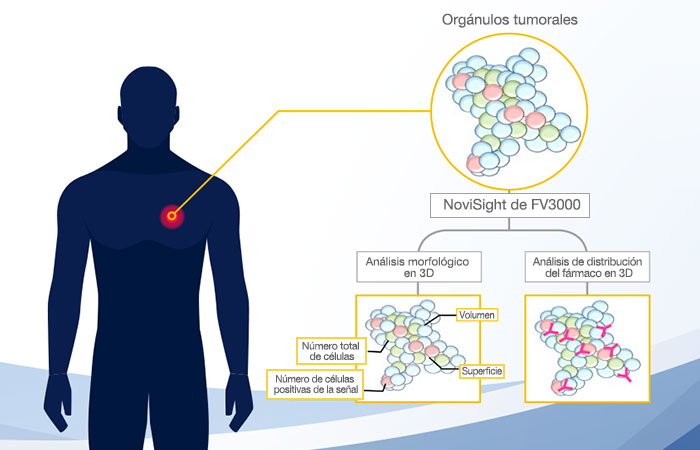
Análisis 3D de orgánulos tumorales derivados de paciente
Las imágenes confocales de los orgánulos tumorales derivados de paciente (PDO) fueron analizadas de forma cuantitativa usando el software 3D NoviSight™ para evaluar las características morfológicas y la unión al anticuerpo de los fármacos moleculares estudiados.
Introducción
Los modelos de tejidos 3D suelen ser usados para el descubrimiento de fármacos debido a que simulan el microentorno in vivo. Los PDO son una de las herramientas más potentes para recapitular la respuesta original del fármaco en el paciente. De hecho, un estudio reciente revela que el perfil fenotípico y genotípico de los PDO cuentan con un alto grado de similitud con el tumor original del paciente. Y, lo que es más importante, los PDO pueden predecir la reactividad del fármaco con una precisión superior al 80 %.
El uso combinado de los orgánulos tumorales derivados del paciente Fukushima, el microscopio de escaneo láser confocal FLUOVIEW® FV3000 de Olympus y el software de análisis 3D NoviSight favorece un novedoso flujo de trabajo para la morfología de los PDO y la distribución del fármaco.
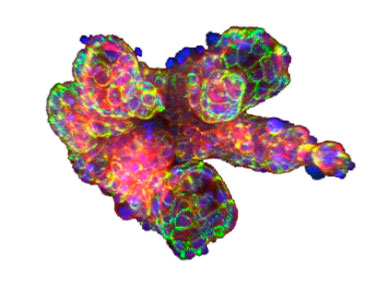
Resumen gráfico
Beneficios
- Visualice y analice los PDO sin perder la información sobre su estructura 3D.
- El software NoviSight puede identificar objetos 3D, clasificar los objetos y proporcionar datos estadísticos.
Métodos
Preparación celular
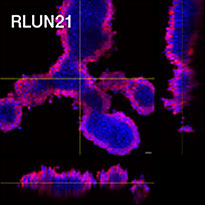
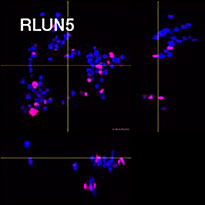
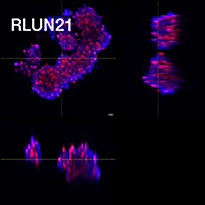
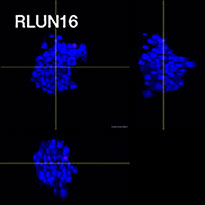
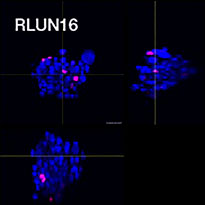
Para preparar las células, se usaron tres modelos F-PDO de pulmón (RLUN5, RLUN16 y RLUN21). El RLUN5 se obtuvo de un tumor carcinoma adenoescamoso, mientras que los modelos RLUN16 y RLUN21 fueron obtenidos de un tumor de carcinoma escamoso. El RLUN21 forma grandes agregados celulares y cuenta con un citoplasma más grande que el resto (Fig. 1).
A continuación, los F-PDO se centrifugan, recopilan y fijan con paraformaldehído al 4% durante la noche. Erbitux®, un inhibidor receptor del factor de crecimiento epidérmico (EGFR) y Herceptin®, un inhibidor del receptor 2 del factor de crecimiento epidérmico (HER2) se marcaron con HiLyte™ Fluor 555 (Chemical Dojin) y se incubaron con los modelos F-PDO durante tres horas.
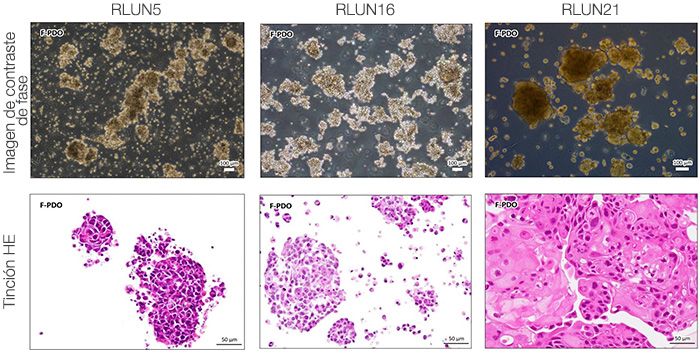
Figure 1 F-PDOs
Inmunotinción y lavado
Se llevó a cabo el protocolo de inmunotinción de Hama et al. con algunas modificaciones (Fig. 2). Cada P-PDO fijado se incubó durante la noche con un anticuerpo Ki67 (Abcam, 16667) y se diluyó con una solución AbScale (0,33 M Urea y 0,2% Triton-X100). Después del lavado con AbScale, los modelos F-PDO se incubaron con un segundo anticuerpo durante tres horas y se les diluyó con AbScale. Después del lavado con la solución de enjuague AbScale durante una hora, los F-PDO volvieron a ser fijados con paraformaldehído al 4 %. Después se lavaron con una solución salina amortiguada por fosfatos (PBS) y se incubaron durante la noche usando el reactivo de lavado ScaleS4 con DAPI. Por último, los modelos F-PDO aclarados fueron observados con el microscopio de escaneo láser confocal FV3000 de Olympus.
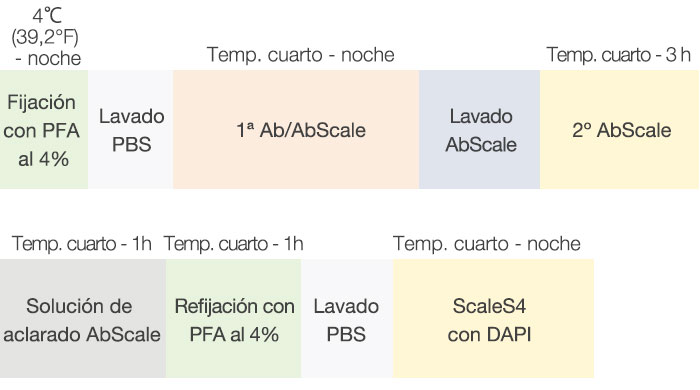
Figura 2: Esquema de inmunotinción y lavado de modelos F-PDO
Procesamiento de imágenes y análisis
Se utilizó una magnificación de 10x o 30x con un paso Z de 2 μm para capturar imágenes de los modelos F-PDO aclarados para el análisis 3D.
Determinar un ajuste de paso Z adecuado es importante para un análisis celular 3D preciso. A continuación, las imágenes se importaron al software NoviSight™ y se reconstruyeron en 3D. El software NoviSight puede reconocer objetos 3D, como núcleos, y convertirlos en datos cuantitativos.
Resultados
Cuantificación 3D de la morfología F-PDO
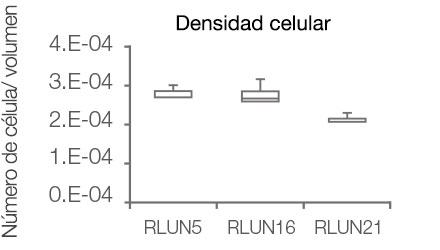
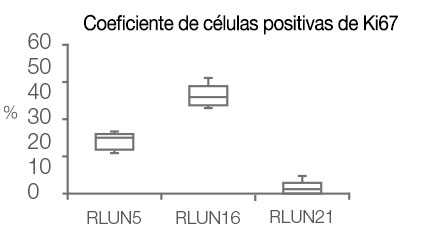
El software NoviSight permitió cuantificar los modelos PDO usando varias imágenes de plano Z. Al teñir los núcleos, el software de análisis capturó la estructura completa y permitió reconocer las células individuales (Fig. 3A). También agregó cada objeto reconocido al gráfico a modo de trama única. Cuando el software reconoció cada núcleo como un objeto, se extrajeron las células positivas Ki67 de forma gráfica y tridimensional creando una pasarela con las tramas Ki67 de alta intensidad (Fig. 3B). Usando estos métodos pudimos cuantificar el número de células de los F-PDO, su volumen, densidad celular y proporción de células positivas Ki67 (Fig. 3C). Se detectó que la proporción positiva de Ki67 del modelo RLUN21 era más baja que las otras. Asimismo, el modelo RLUN21 con el citoplasma más grande podría haber provocado su densidad celular inferior.
A | |||
 RLUN21 original | 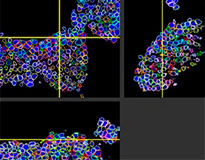 Reconocimiento nuclear | 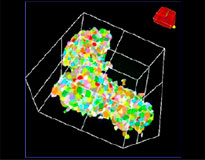 Vista volumétrica de reconocimiento nuclear | 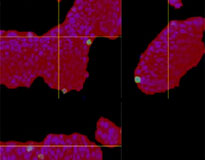 RLUN21 |
B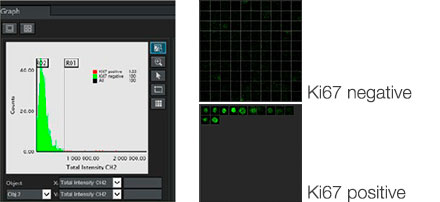 | C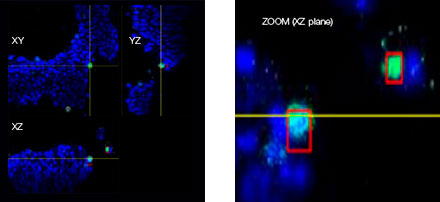 |
D
| RLUN5 | RLUN16 | RLUN21 | |
| número de célula | 926 (±719) | 294 (±162) | 2595 (±1480) |
| volumen (vóxeles) | 3.35.E+06 (±3.26.E+06) | 1.08.E+06 (±6.85.E+05) | 1.13.E+07 (±9.12.E+06) |
 |  |
| Figura 3 Cuantificación 3D de la morfología de los modelos F-PDO | |
A. Vistas originales de los tres lados del modelo RLUN21; reconocimiento nuclear 3D de NoviSight (vista volumétrica, y tres lados) y reconocimiento estructural del NoviSight.
B. Las células positivas/negativas de Ki67 fueron ordenadas por intensidad de Ki67. El software NoviSight puede visualizar las células ordenadas en una «Vista de galería».
C. Las células positivas y clasificadas de Ki67 pueden ser visualizadas 3D con un círculo rojo.
D. Datos cuantitativos de los modelos F-PDO.
Análisis de distribución de fármacos 3D
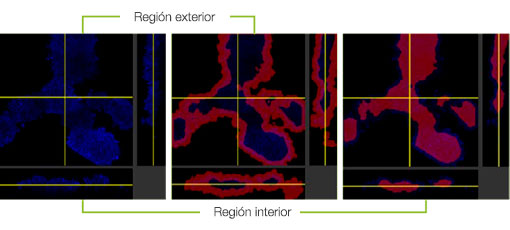
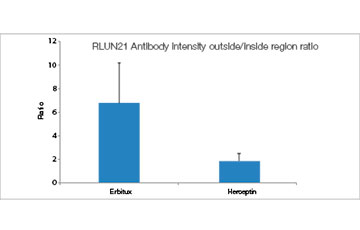
Cuando se añadió Erbitux o Herceptin etiquetado como HyLight-555 para cada modelo F-PDO, Erbitux se unió de forma uniforme al modelo RLUN21 desde su superficie, mientras que Herceptin se unió de forma irregular al modelo RLUN21. El módulo de reconocimiento volumétrico del software NoviSight™ permitió cuantificar el índice de volumen positivo del fármaco de anticuerpos (Fig. 4A). A continuación, se usó el software NoviSight para cuantificar la diferencia en los estilos de unión, ya que puede modificar la región destinada al análisis. Para ello, se crearon dos regiones focalizadas: una región de volumen reducido a partir de la superficie con un porcentaje específico y una región de volumen de contorno de cualquier ancho/anchura. Se calculó la intensidad del fármaco de anticuerpos durante los volúmenes. Se observó una gran diferencia cuantitativa entre el volumen reducido y el volumen de contorno con el Erbitux, mientras que la diferencia era pequeña con el Herceptin. Esto significa que el Erbitux se une fuertemente a la región de contorno del modelo RLUN21 mientras que el Herceptin se une al modelo RLUN21 sin sesgos. Este método nos permitió mostrar cuantitativamente la distribución del fármaco de anticuerpos.
A
 |  |
| Reconocimiento volumétrico del fármaco de anticuerpos 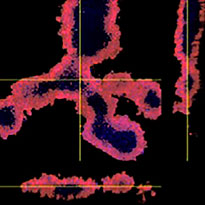 |
|
 |
| Reconocimiento volumétrico del fármaco de anticuerpos 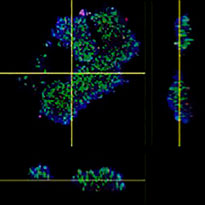 |
Volumen positivo de anticuerpos (%)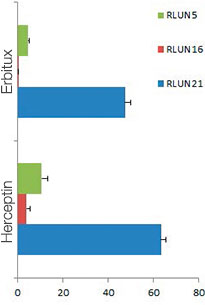
B
 |  |
| Figura 4 Cuantificación 3D de la distribución del fármaco de anticuerpos |
A. Imágenes de los tres lados de los modelos F-PDO con Erbitux o Herceptin, y reconocimiento de las uniones del fármaco de anticuerpos con el NoviSight. El gráfico muestra el volumen de unión de los anticuerpos en toda su medida.
B. Módulo de modificación de la región con NoviSight. NoviSight puede modificar la región dedicada al análisis para proporcionar datos cuantitativos en una región limitada.
Conclusión
A través de este estudio, se ha revelado que el software NoviSight puede analizar de forma cuantitativa modelos PDO a nivel morfológico y farmacológico respaldado por imágenes capturadas con el microscopio de escaneo láser confocal FV3000 de Olympus. La combinación de las imágenes en alta resolución del microscopio FV3000 con la alta precisión de reconocimiento del software NoviSight, se pudieron generar resultados cuantitativos más fiables.
Referencias
- Vlachogiannis G et al., (2018) Patient-derived organoids model treatment response of metastatic gastrointestinal cancers. Science. 359(6378):920-926. doi: 10.1126/science.aao2774
- Takahashi et al., (2019) An In Vitro System for Evaluating Molecular Targeted Drugs Using Lung Patient-Derived Tumor Organoids. Cells. 8(5), 481. doi:/10.3390
- Tamura H, et al. Evaluation of anticancer agents using patient-derived tumor organoids characteristically similar to source tissues. Oncol Rep.,40, 635-646, 2018
- Hama et al., (2016) Deep Imaging of Cleared Brain by Confocal Laser-Scanning Microscopy. Nature Protocol Exchange. doi:/10.1038 Mayu
Autores
Mayu Ogawa (Olympus)
Reconocimiento
Este estudio ha sido apoyado por el Profesor Takagi de la Universidad Médica de Fukushima. Para obtener más información sobre los modelos F-PDO (orgánulos derivados de paciente de Fukushima), visite https://www.fmu.ac.jp/home/trc/en/contract-research-provision/f-pdo/
Productos usados para esta aplicación
se ha añadido correctamente a sus marcadores
Maximum Compare Limit of 5 Items
Please adjust your selection to be no more than 5 items to compare at once
Not Available in Your Country
Sorry, this page is not
available in your country.