Análisis de imágenes fluorescentes: División celular en esferoides
Es posible visualizar la división celular dentro de los esferoides al teñir el núcleo celular y los microtúbulos. El número de células en mitosis de los esferoides puede ser evaluada de forma cuantitativa usando las imágenes capturadas por el microscopio confocal láser y el módulo de recuento del software NoviSight™.
Objetivos
El grado de malignidad del tejido canceroso se evalúa midiendo el número de células en mitosis o las células en mitosis atípica. El número de células cancerosas en mitosis suele determinarse mediante la citometría de flujo. Esta técnica permite disociar el tejido canceroso y el núcleo teñido para contar el número de células en mitosis, independientemente de si se encuentra en un cultivo celular 2D o 3D. Sin embargo, como la citometría de flujo no puede visualizar las estructuras originales de los tejidos en 3D, resulta imposible identificar la localización de las células en mitosis dentro del tejido canceroso. También resulta complejo analizar la relación entre la información morfológica, como el tamaño del tumor y la división celular. En este estudio, se consiguió visualizar correctamente las células mitóticas dentro de un esferoide tumoral intacto al teñir el núcleo y el microtúbulo seguido del lavado del tejido. Esta técnica, combinada con el software NoviSight™, nos permitió contar el número de células en mitosis. El análisis cuantitativo de las imágenes permitió identificar la ubicación de las células en mitosis y las que se encontraban en una mitosis atípica.
Preparación de las muestras
Se cultivó una suspensión celular de HT-29 en una placa PrimeSurface® 96U (SUMITOMO BAKELITE CO., LTD) con una proporción de 500 células/pocillo. Después de 5 días de cultivo, las células formaron una estructura esferoide, y se trataron los esferoides con diversas concentraciones de Paclitaxel. Después de la adición de Paclitaxel, los esferoides se incubaron durante 48 horas y se fijaron con paraformaldehído al 4 %. El núcleo celular y los microtúbulos fueron teñidos con Hoechst33342 (DOJINDO) y anticuerpos antitubulina conjugados con Alexa Fluor 488 (eBioscience), respectivamente. Los esferoides teñidos fueron trataron con un reactivo de lavado de tejido, ScaleS; y, se dejó actuar durante la noche a 37 ºC.
Conclusión
Adquisición y análisis de imágenes fluorescentes
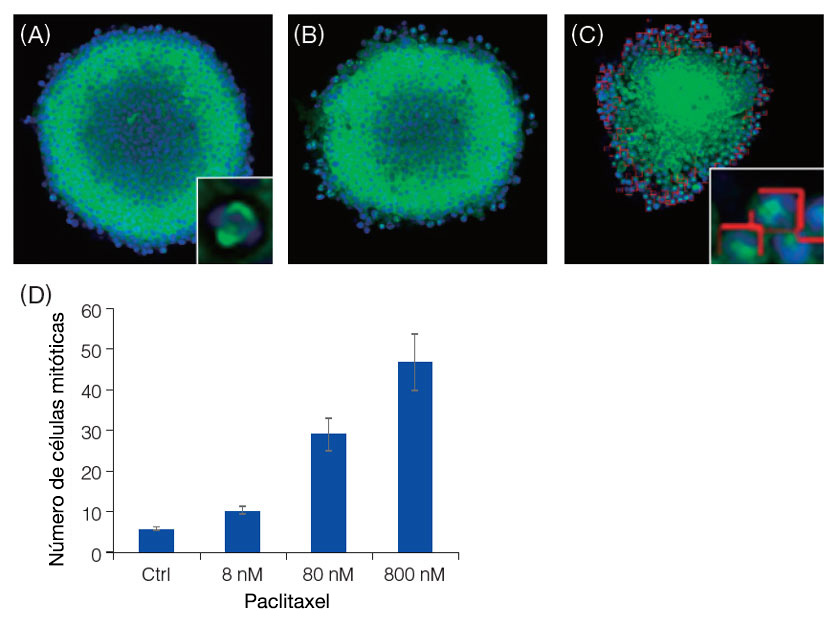
Las imágenes fluorescentes de los esferoides se obtuvieron usando el microscopio de escaneo láser confocal FV3000. En el grupo de control sin tratamiento, se observó la formación de husillos por los microtúbulos, una característica específica de las células en mitosis, en tres capas celulares de la superficie del esferoide (A). El software NoviSight™ fue utilizado para contar el número de células en mitosis en el grupo de control y en el grupo tratado con Paclitaxel (grupos B y C). Los resultados indican que el Paclitaxel aumentaba el número de células en mitosis de forma supeditada a la concentración (D). Los resultados indican claramente el efecto del Paclitaxel como inhibidor de despolimerización de microtúbulos.
PrimeSurface es una marca registrada de Sumitomo Bakelite Co., Ltd.
Olympus es una marca registrada, y NoviSight and Insightful Analysis, Intelligent Answers son marcas comerciales de Olympus Corporation.
Productos usados para esta aplicación
se ha añadido correctamente a sus marcadores
Maximum Compare Limit of 5 Items
Please adjust your selection to be no more than 5 items to compare at once
Not Available in Your Country
Sorry, this page is not
available in your country.
