TruAI™ ディープラーニングは画期的な画像解析手法で、かつては不可能または困難だったアプリケーションに研究者が取り組めるようになっています。例えば、信頼性の高いラベルフリー解析や、非常に輝度の低い生細胞のトラッキングが数日にわたって可能です。
このようなアプリケーションでは、セマンティックセグメンテーションによって解析を実行します。これは、ピクセルが特定クラスの背景または前景に属するかを特定する機能です。 セマンティックセグメンテーションの後、watershed(分水嶺)などの後処理ステップを適用し、最終的なオブジェクトセグメンテーションを行います(通常は核または細胞全体)。
TruAIはインスタンスセグメンテーションの導入により改善されました。 この機能は、セマンティックセグメンテーションとそれに続くオブジェクト分離をひとつのステップにまとめることができます。 インスタンスセグメンテーションではワークフローが改善され、後処理の分離ステップを必要とする細胞コロニー内の細胞のセグメンテーションといった、難しいアプリケーションにもワンステップで対処できます。
TruAIディープラーニングによって、ユーザーは最初からユーザー自身のデータで学習できるため、生成されるTruAIディープニューラルネットワーク(DNN)モデルの性能は非常に優れたものになります。 研究者はさまざまなアプリケーション用にDNNのライブラリーを作成することも、共同作業者と共有することもできます。
これはディープラーニングワークフローが必ず以下の3つのステップから構成されることを意味します。
- ユーザー自身のデータでのラベリング
- 学習
- 推論
当社のソフトウェアを使用しても、ラベリングステップは最も時間のかかる作業です。特に、よい性能を発揮するためにたくさんのオブジェクトにラベリングする必要があり、難しいアプリケーションの場合は時間がかかります。
事前学習ディープラーニングモデルを使用した細胞と核の簡単なセグメンテーション
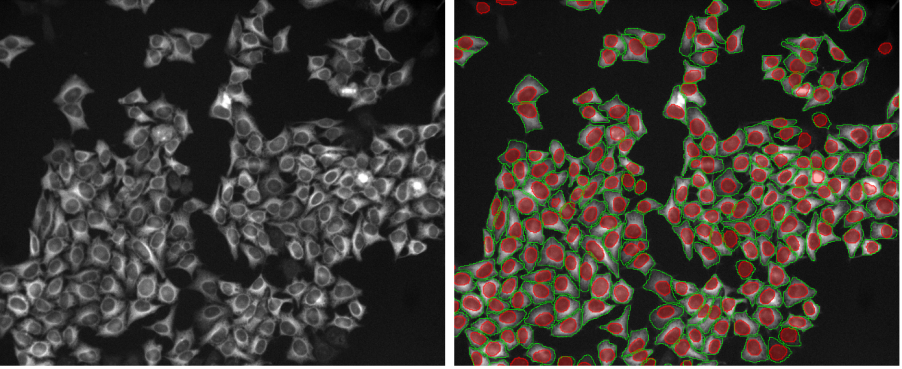
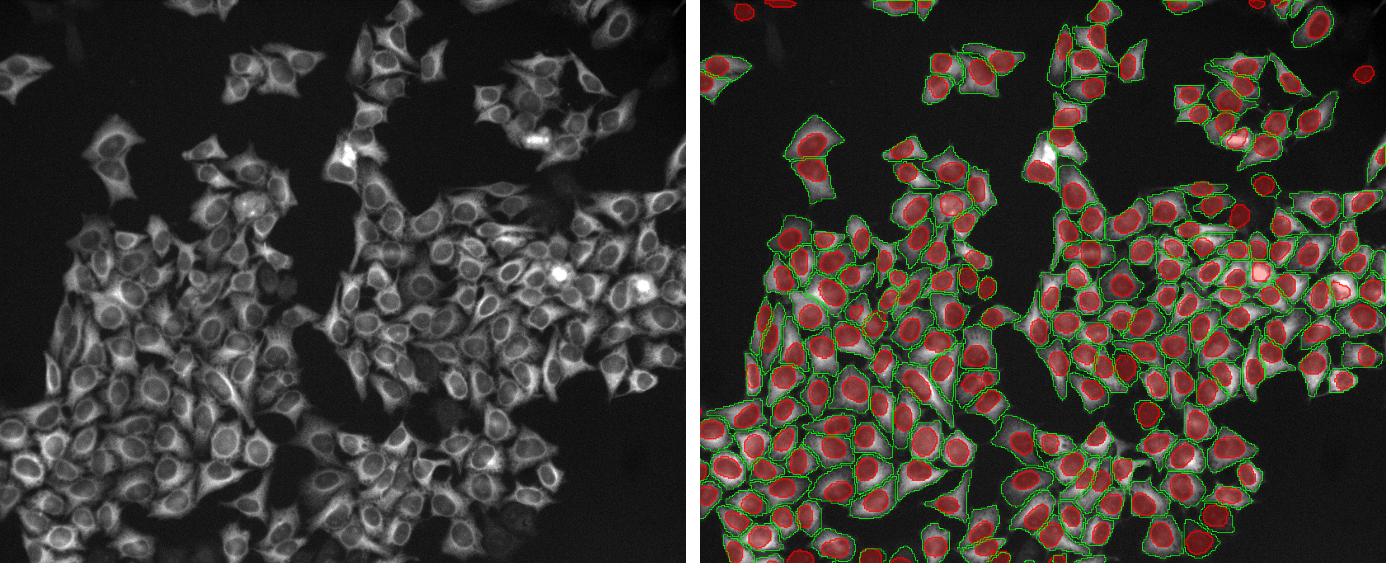
このワークフローを改善するため、TruAIディープラーニングには、核と細胞の事前学習モデルがいくつか組み込まれるようになりました。核と細胞は、生物画像解析において最も一般的なセグメンテーション対象オブジェクトです。 この結果、ユーザーはラベリングと学習に費やす時間を短縮できます(図1)。

図1: 学習や推論に、独自データとともにTruAIディープラーニングを使用して最適な性能が得られるようになります。 より早い方法として、事前学習されたTruAIモデルを使用すれば、ワンクリックするだけで解析を実行できます。
核と細胞のTruAI事前学習モデルは、以下のようにさまざまな条件の蛍光画像に対してインスタンスセグメンテーションを実行するように学習されています。
- 顕微鏡法(ポイントスキャン型共焦点、スピニングディスク型共焦点、ワイドフィールド)
- 染色(DAPI、ファロイジン、 MitoTracker、Laminなど)
- 細胞株(HeLa、U2OS、SK-HEP-1、植物細胞、組織など)
- コントラスト、SN比、背景レベル
- 画素分解能と倍率
注意すべき点は、事前学習モデルは汎用モデルであり、すべての状況で完璧にセグメンテーションを実行できるわけではないということです。 これらのモデルの能力をわかりやすくするため、細胞セグメンテーションシナリオのリストをまとめてみました。
事前学習されたディープラーニングモデルを使用して核と細胞のセグメンテーションを行った20の例
以下の画像(図2、a~t)は、さまざまなセグメンテーションシナリオにおける核(赤)と細胞(緑)のTruAI事前学習モデルの実例を示しています。 これには、各種の細胞株、マーカー染色、倍率、分解能、コントラスト、SN比、背景不均一性が含まれます。 両方のモデルを同じ画像に適用できます(図2、p~t)。 また、モデルを非特異核(図2、q~t)や細胞の染色(図2p、s)に適用することもできます。
1. U2OS細胞、核染色、ワイドフィールド20x、中密度でさまざまなサイズと形態の細胞を含む
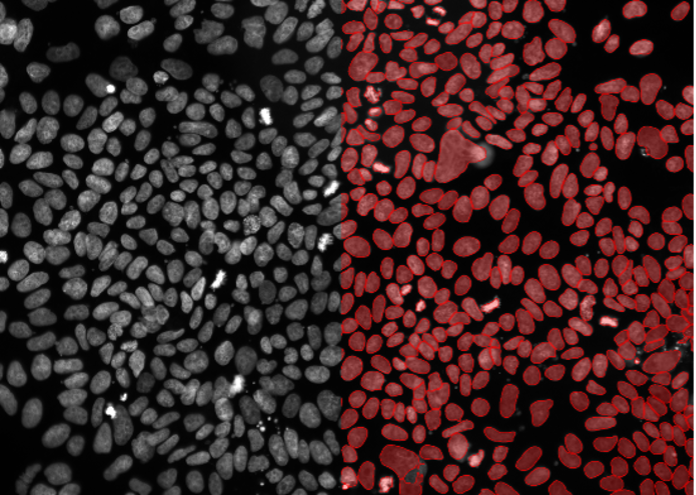
図2a
2. HeLa細胞、核染色、ワイドフィールド10x、不均一な背景
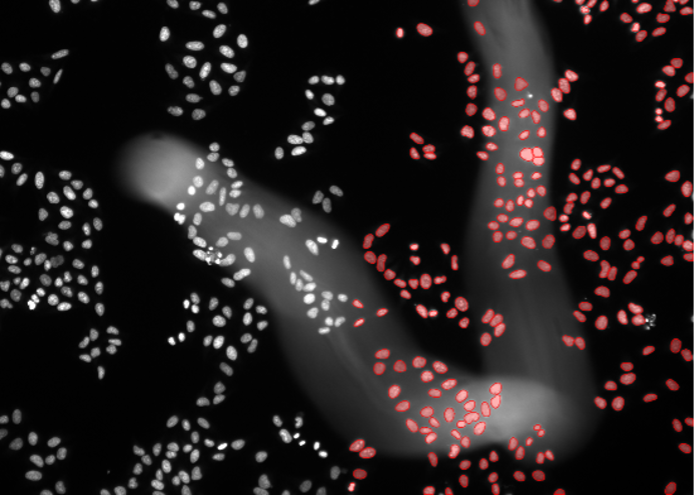
図2b
3. 多能性幹細胞、核マーカー、ワイドフィールド20x、非常に高密度

図2c
4. 腎臓オルガノイド細胞、核染色、スピニングディスク型共焦点30x、高い浸透深度
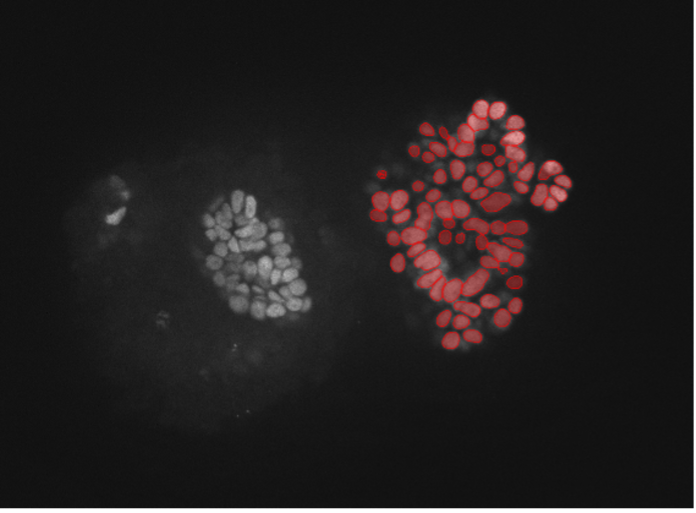
図2d
5. HeLa細胞、核染色、スピニングディスク型共焦点40x、高コントラスト、高分解能

図2e
6. A549ヒトがん細胞、核マーカー、スピニングディスク型共焦点40x、低SN比
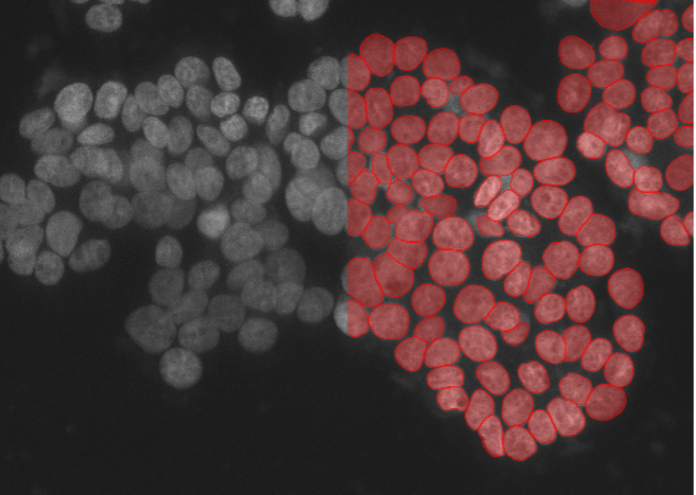
図2f
7. ヒト組織腫瘍細胞、核染色、ワイドフィールド20x

図2g
8. マウス腎臓組織細胞、核染色、ワイドフィールド20x、厚い標本

図2h
9. Rat-1細胞、細胞質染色、ワイドフィールド10x、高い細胞密度
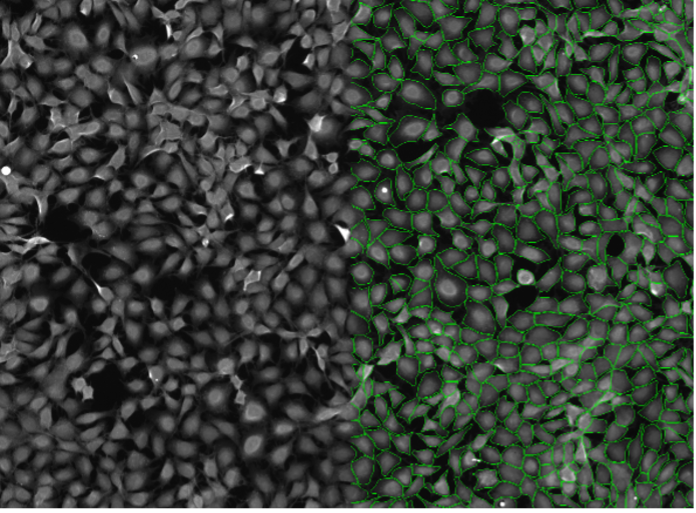
図2i
10. SK-HEP-1細胞、細胞コントラスト染色、ワイドフィールド20x
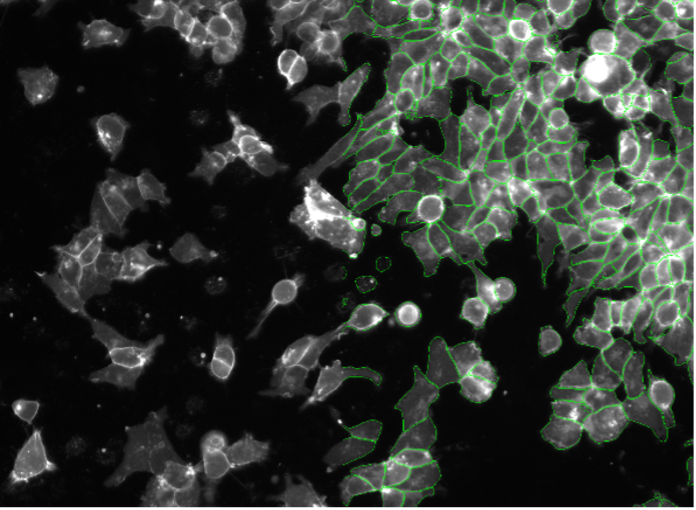
図2j
11. 植物細胞、自家蛍光、ワイドフィールド20x、低SN比
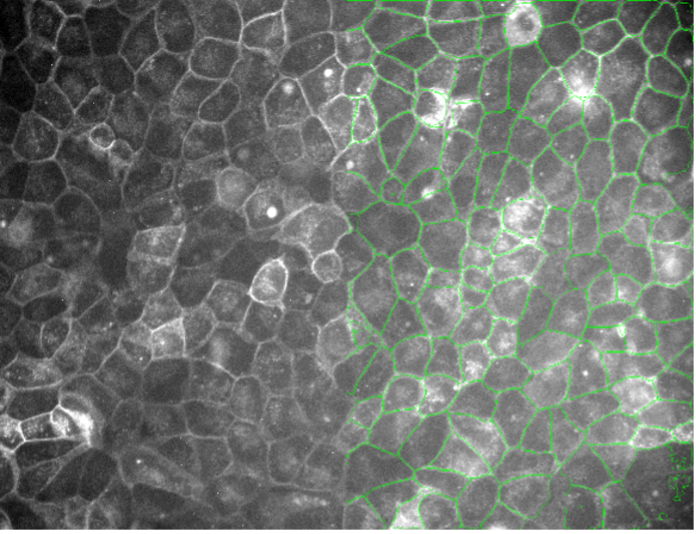
図2k
12. HeLa細胞、核膜染色、ワイドフィールド20x
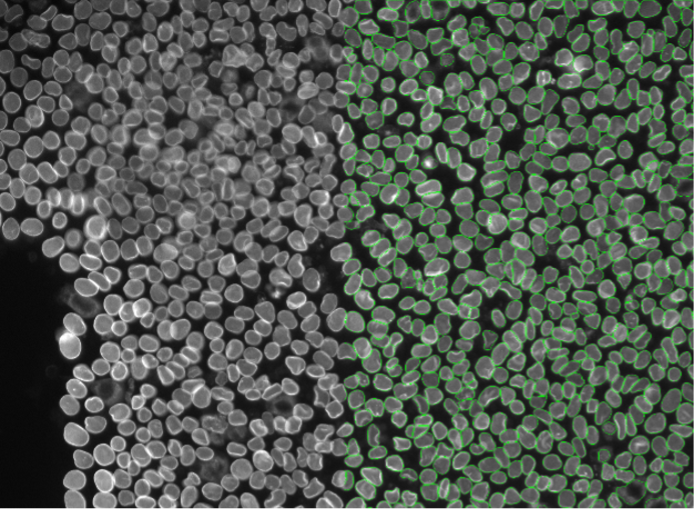
図2l
13. huFIB細胞、チューブリン染色、ワイドフィールド20x
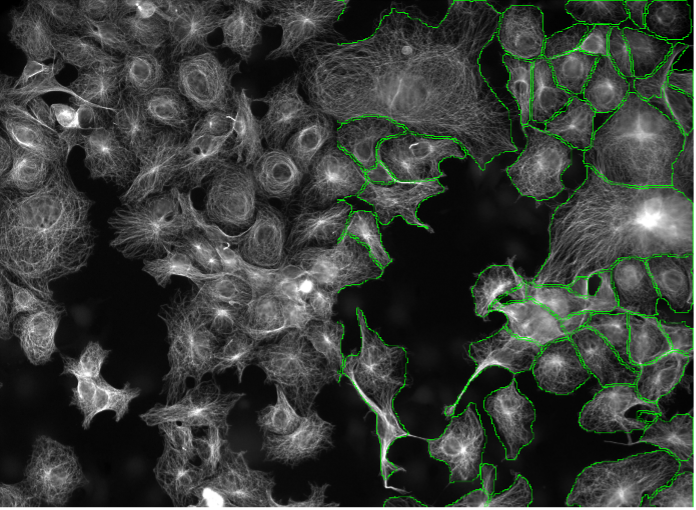
図2m
14. Rat-1細胞、アクチン染色、ワイドフィールド20x
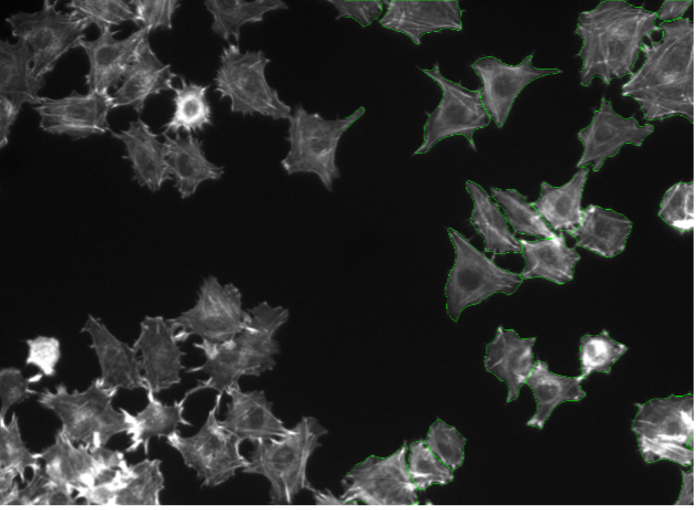
図2n
15. BPAE細胞、アクチン染色、ポイントスキャン型共焦点40x
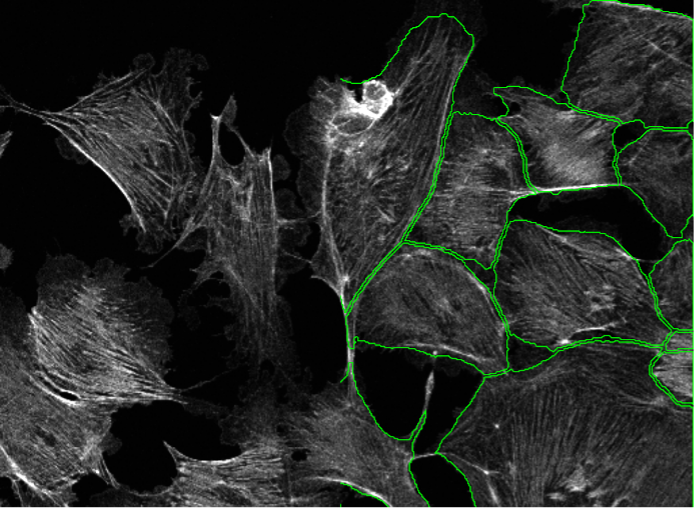
図2o
16. Rat-1細胞、細胞質に滲み出ている核染色、ワイドフィールド20x
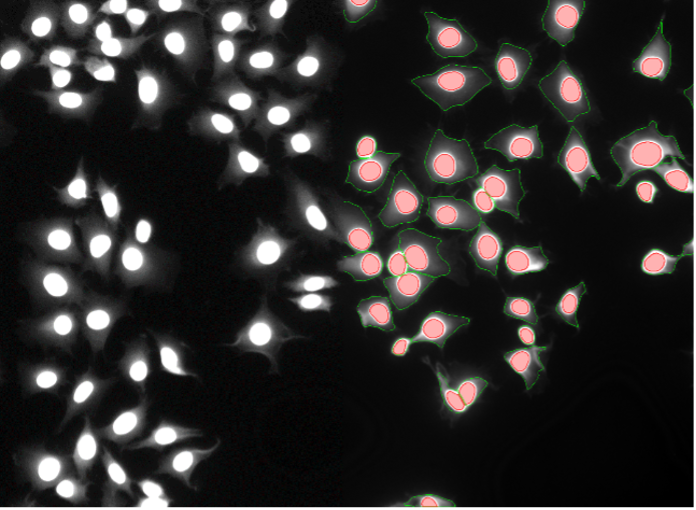
図2p
17. HeLa細胞、チューブリン染色、ワイドフィールド4x、低分解能、低SN比

図2q
18. Rat-1細胞、細胞質染色、ワイドフィールド20x
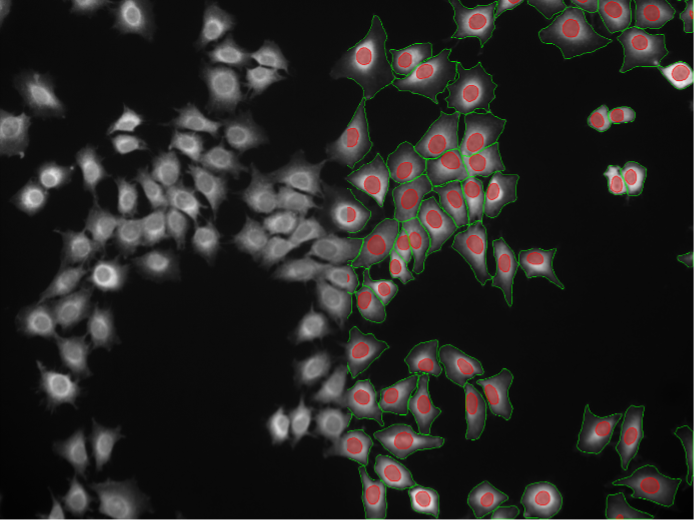
図2r
19. COS-7細胞、ミトコンドリア染色、ポイントスキャン型共焦点40x
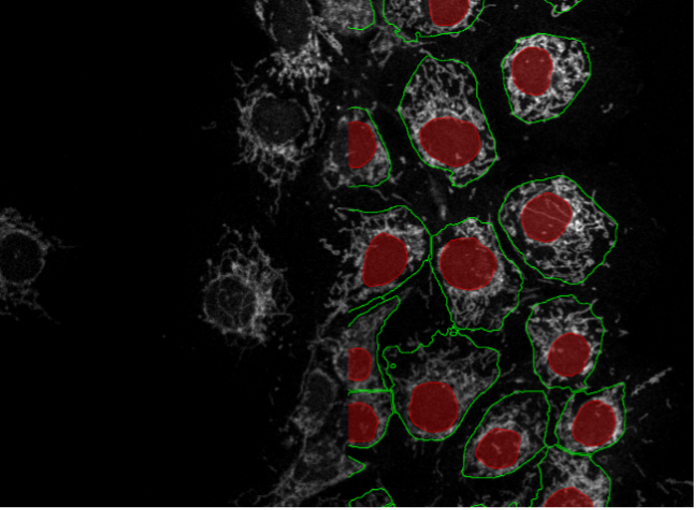
図2s
20. BPAE細胞、チューブリン染色、ポイントスキャン型共焦点40x
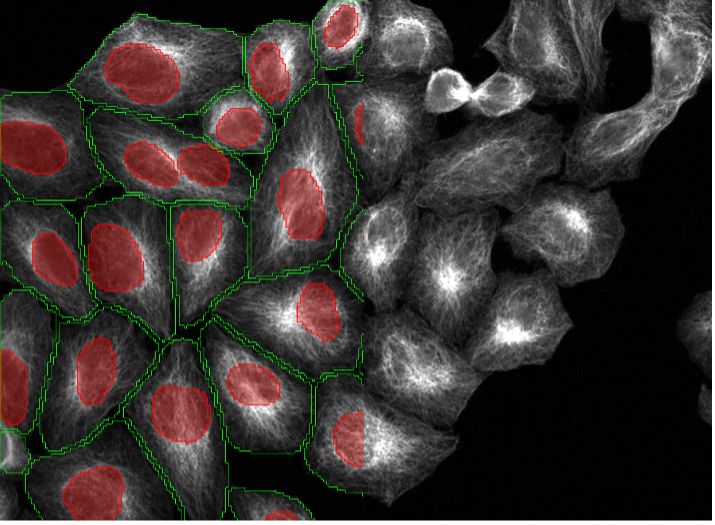
細胞と核のセグメンテーション向けに強化されたディープラーニング機能
インスタンスセグメンテーションと事前学習モデルの導入によって、TruAI ツールセットの機能が強化されています。 事前学習モデルから始めて、細胞と核のセグメンテーションはワンクリックで実行されるので、時間を節約できます。 結果が適正でない場合は、TruAIによる予測を新たなラベルに変換して、修正内容を適用することができます。 修正されたラベルが新たな学習のベースになるので、時間と労力が節約されます。
当社のお客様は、強化されたディープラーニング機能の利点を既に認めています。 Danish Cancer Society Research Centerのシニアサイエンティスト、Robert Strauss氏は次のように述べています。「事前学習された核の識別は実に素晴らしく、非常に不均一なサンプルでも、細胞分離を損なわずに容易に解析できます。 特に、細胞密度が高い領域におけるTruAIベースの分離は、速さと性能の両面で、輝度やエッジ検出よりも明らかに優れています」
関連コンテンツ
ディープラーニングで細胞と核のインスタンスセグメンテーションを簡単に