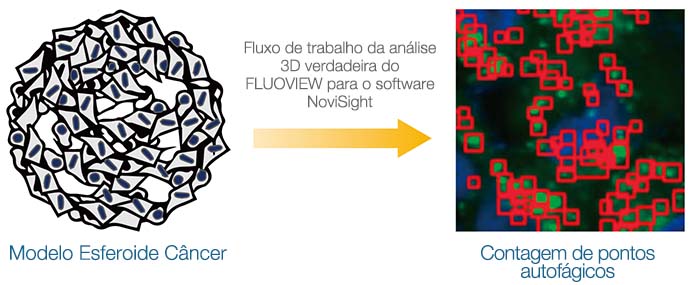
Análise 3D verdadeira de uma via autofágica intracelular em um modelo esferoide 3D
Resumo
Modelos de cultura 3D têm sido usados para prever a eficácia ou toxicidade de medicamentos. Nesta nota de aplicação, focamos em uma via autofágica intracelular. Primeiramente, confirmamos a utilidade da sonda EGFP-LC3 para monitorar o status autofágico dos modelos Em seguida, o processo de trabalho de análise 3D verdadeira da Olympus usando o microscópio confocal FLUOVIEW™ FV3000 e o software NoviSight™ foi usado para avaliar quantitativamente o efeito de um candidato a medicamento chamado cloroquina. Nós demonstramos que esse processo de trabalho da análise oferece uma alternativa para traçar o perfil de candidatos a medicamentos usando estudos in vivo.
Introdução
Os eventos moleculares intracelulares estão intimamente relacionados a uma ampla variedade de patologias em humanos. A autofagia é um processo intracelular que degrada e recicla organelas e proteínas celulares, e a desregulação da autofagia está implicada em doenças humanas. Para compreender melhor esses processos de doenças e testar a eficácia dos medicamentos neles, é importante monitorar o estado autofágico das células humanas sob condições patológicas e terapêuticas.
Modelos de cultura 3D, como esferoides ou organoides, assemelham-se muito ao complexo microambiente in vivo. Para avaliar a eficácia de um medicamento nas células do esferoide, é fundamental analisar quantitativamente as imagens microscópicas intracelulares. Nesta nota de aplicação, avaliamos um processo de autofagia intramolecular dinâmico e avaliamos quantitativamente o efeito de um candidato a medicamento usando o microscópio confocal FV3000 da Olympus e o processo de trabalho da análise 3D verdadeira do software de análise NoviSight.
Benefícios
- Análise quantitativa de eventos intramoleculares em modelos de cultura 3D
Resultados e discussão
Uma proteína LC3 é um marcador útil em um processo de autofagia. Por exemplo, foi relatado que os pontos de fluorescência EGFP-LC3 aumentaram quando os autofagossomos foram acumulados. A formação de autofagossomos é regulada por vários compostos que modulam as atividades autofágicas ou a movimentação dos autofagossomos. Alguns desses compostos estão agora em testes clínicos. Um deles, a cloroquina (CQ), originalmente um medicamento antimalárico, está agora em um ensaio clínico para tratamento de câncer porque inibe a fusão de autofagossomos e lisossomos.
Validação de um marcador de autofagia usando um sistema de cultura 2D
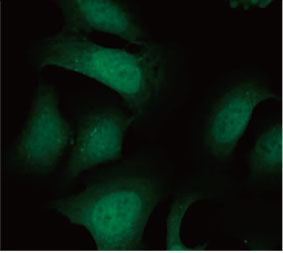
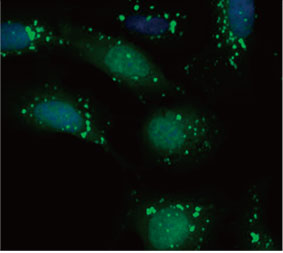
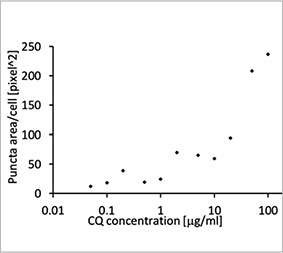
Nós validamos a utilidade de uma sonda EGFP-LC3 para medir o efeito inibitório do CQ no processo autofágico em um sistema de cultura 2D. Preparamos uma linha de células de osteossarcoma U2OS expressando de forma estável EGFP-LC3. As células foram cultivadas como monocamadas em poços de microplaca. Depois de adicionar a CQ, as células foram fixadas e coloridas com Hoechst 33342. Imagens fluorescentes mostraram que o tratamento com CQ evocou a formação de puncta EGFP-LC3 (Figura 1 A e B). A área de puncta por célula foi medida com base na posição do núcleo de cada célula. A área de puncta aumentou conforme a concentração de CQ aumentou, confirmando a utilidade da sonda EGFP-LC3 para medir um processo autofágico.
(A)
| (B)
| (C)
|
Figura 1 A e 1 B: (A) células U2OS que expressam EGFP-LC3 cultivadas em condições normais. (B) células U2OS expressando EGFP-LC3 tratadas com CQ por 1 hora. Figura 1 C: O aumento da área de puncta por célula representada graficamente com o aumento da concentração de CQ. | ||
Quantificação de LC3 pontilhado no modelo de esferoide tumoral
Para monitorar o estado autofágico em modelos de cultura 3D, selecionamos uma linha de células HeLa estabelecida a partir de carcinoma cervical. As células HeLa são adequadas para um protocolo de cultura 3D sem estrutura e formam esferoides tumorais de tamanho uniforme. Preparamos uma linha de células de HeLa expressando de forma estável EGFP-LC3.
As células foram semeadas em microplacas de fundo redondo de baixa fixação. Após cinco dias de cultura, os esferoides foram tratados com CQ por sete horas. Em seguida, os esferoides foram fixados, permeabilizados por membrana, seus núcleos tingidos e, finalmente, limpos com SCALEVIEW-S4 (FUJIFILM WAKO).
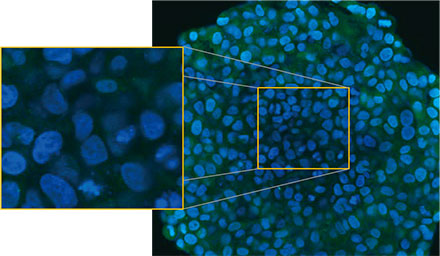
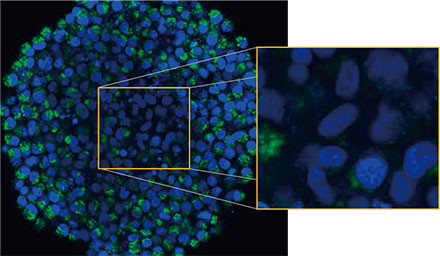
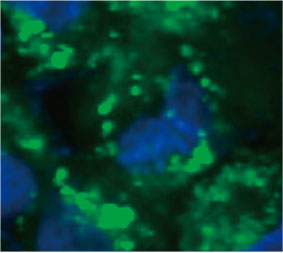
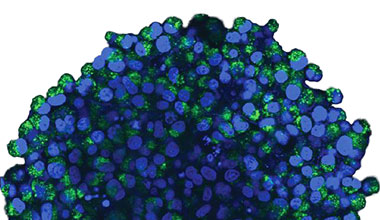
Observamos os esferoides usando o sistema confocal FLUOVIEW™ FV3000 da Olympus. Usamos uma objetiva de imersão em silicone (UPLSAPO30XSIR) devido à sua alta abertura numérica (AN) e redução da aberração esférica. A Figura 2 (A)* mostra uma imagem de fatia Z única do esferoide não tratado no equador. O sinal EGFP apareceu uniformemente nas células. Em contraste, o tratamento com CQ induziu a formação de sinais EGFP de puncta nas células (Figura 2 (B)*). As formações em pontos foram observadas tanto na zona periférica quanto na zona central do esferoide. O tratamento com CQ não causou nenhuma mudança aparente no tamanho do esferoide, indicando que o processo autofágico intracelular pode ser um marcador melhor para avaliar a eficácia do CQ em esferoides tumorais 3D.
Para analisar quantitativamente os eventos intracelulares nos modelos de cultura 3D, usamos o processo de trabalho da análise 3D verdadeira da Olympus que combina imagens capturadas usando o microscópio confocal FV3000 e da análise usando o software NoviSight™, que oferece muitos benefícios em relação aos métodos analíticos convencionais. Em uma análise convencional, usaríamos o valor de característica integrado dos objetos reconhecidos de várias imagens de corte Z ou analisaríamos a imagem de projeção de várias imagens de corte Z. Esses métodos não são confiáveis porque podem levar a contar várias vezes os objetos de interesse ou perder os objetos de interesse que foram sobrepostos e obscurecidos por outros objetos. Em contraste, o processo de trabalho da análise 3D verdadeira da Olympus inclui a aquisição de imagens sequenciais de fatias Z com intervalos Z otimizados pelo software FLUOVIEW™. O software reconstruiu o volume 3D e reconheceu os objetos de interesse como conjuntos de modelos. O software NoviSight é então usado para análises estatísticas. O processo de trabalho do FLUOVIEW para o software NoviSight é direto e oferece uma plataforma ideal para a análise de modelos de cultura 3D.
(A)
| (B)
|
Figura 2 A e 2 B: esferoides de células HeLa que expressam EGFP-LC3 (A) em condição normal e (B) tratados com CQ. As imagens ampliadas mostram a região do retângulo amarelo das imagens esferoides originais.* | |
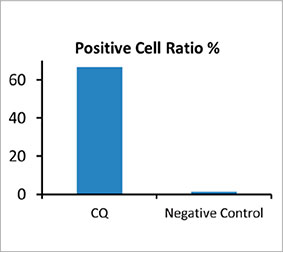
Para calcular o número de células positivas para autofagia no esferoide, o software identificou o núcleo de cada célula. Em seguida, as regiões ao redor de cada núcleo foram definidas como regiões de máscara. Finalmente, os pontos dos sinais EGFP nas regiões de máscara foram reconhecidos como objetos em pontos (Figura 2 (C)*). As células que têm mais de três pontos foram consideradas células positivas para autofagia. O esferoide 3D sem tratamento com medicamentos apresentou cerca de 1,4% de células autofagicamente positivas, enquanto o esferoide tratado com CQ apresentou 66,6% de células autofágicas positivas (Figura 2 (D)*). A análise quantitativa também confirma que a CQ induziu a formação de pontos nos esferoides do câncer.
(C)
|
| (D)
|
Figura 2 C à esquerda: A imagem original das células no esferoide com CQ. À direita: A mesma imagem com reconhecimento de objeto para pontos (retângulos vermelhos).* | ||
Conclusão
O microscópio confocal FLUOVIEW FV3000 da Olympus e o software NoviSight, como parte de um processo de trabalho de análise 3D verdadeira, foram usados para avaliar quantitativamente o efeito da CQ no processo de autofagia intracelular em modelos de cultura 3D. Este estudo demonstra que os pesquisadores podem usar esse processo de trabalho para traçar o perfil da eficácia do medicamento de uma maneira dependente da dose ou selecionar vários candidatos a medicamentos de forma objetiva. Existem outros marcadores moleculares intracelulares que são relevantes para a eficácia ou toxicidade do medicamento, como sinais de FISH nos cromossomos ou translocação de moléculas de sinalização marcadas com fluorescência. Este processo de trabalho pode ajudar a avaliar quantitativamente uma ampla gama de eventos intracelulares em modelos de cultura 3D e oferece perfis alternativos de candidatos a medicamentos em vez de estudos in vivo.
References
- Maria C et al., (2019) Targeting autophagy to overcome human disease. International Journal of Molecular Sciences. 20(3): E725. doi: 10.3390/ijms20030725
- Yan C et al., (2013) Therapeutic targeting of autophagy in disease: Biology and Pharmacology. Pharmacological Reviews. 65: 1162–1197. doi: 10.1124/pr.112.007120
- Daniel JK et al., (2008) Guidelines for the use and interpretation of assays for monitoring autophagy in higher eukaryotes. Autofagia. 4(2): 151–175. doi: 10.4161/auto.5338
Autor
Kazuhito Goda
*Embora tenha se tornado uma das linhagens celulares mais importantes na pesquisa médica, é importante reconhecer que a contribuição de Henrietta Lacks para a ciência aconteceu sem o seu consentimento. Essa injustiça, embora tenha levado a descobertas importantes em imunologia, doenças infecciosas e câncer, também levantou discussões importantes sobre privacidade, ética e consentimento na medicina.
Para saber mais sobre a vida de Henrietta Lacks e sua contribuição para a medicina moderna, clique aqui.
http://henriettalacksfoundation.org/
Produtos usados nesta aplicação
foi adicionado com sucesso aos seus favoritos
Maximum Compare Limit of 5 Items
Please adjust your selection to be no more than 5 items to compare at once
Not Available in Your Country
Sorry, this page is not
available in your country.