使用共聚焦显微镜应对糖尿病
摘要
解决糖尿病全球挑战的研究工作在很大程度上依赖于采用先进的显微镜技术,但许多研究人员通常无法获得此类设备。为满足生命科学研究的日常需求,一种全新紧凑型多合一共聚焦显微镜的问世让学生和教授们都能够获得高质量的结果。
罗斯托克大学医学系Simone Baltrusch教授的研究小组可以证明,奥林巴斯的FluoView FV10i就是一种深受欢迎的工具。她与奥林巴斯应用专家Helge Schmidt博士会面,讨论了共聚焦显微镜的可拓展选项如何促进她所在小组的工作-增进对线粒体网络作用的理解,并促进神经病诊断技术的发展。
如果按着目前的趋势,预计到2035年将有十分之一的成年人患有糖尿病,这是一种正在日益成为紧迫性医学挑战的疾病。1

团队
Simone Baltrusch教授(后排,中间)和她的研究小组部分成员(从左后到右前:Rica Waterstradt,Julia Schultz博士,Annett Kott博士,Janine Leckelt博士,Jan Niemann博士在实验室中使用奥林巴斯 FluoView FV10i。
引起这种代谢紊乱的关键因素之一是胰腺产生胰岛素的β细胞功能受损,随后胰岛素分泌下降,导致血糖水平异常升高,并造成各种生理并发症。1型糖尿病源于β细胞自身免疫破坏,而2型糖尿病的特征是β细胞衰竭和人体周围组织的胰岛素耐受性。了解这种复杂疾病的机制和意义非常重要,罗斯托克大学医学院的Simone Baltrusch教授发现共聚焦激光扫描显微镜正是实现这一目标的理想工具。
与标准宽视场显微镜相比,共焦激光扫描显微镜可提供仅来自特定焦平面的清晰图像。随着共聚焦技术的发展,有趣的是,尽管复杂模块化系统(如基于多光子技术构建的系统)能够实现最前沿的体内研究,但也出现一种可以满足生命科学研究实验室日常需求的新型紧凑型多合一系统。能够让Simone Baltrusch教授小组的每位成员均能从共聚焦显微镜中受益的系统就是奥林巴斯的FluoView FV10i。她补充说:“我们之所以选择FV10i,是因为并不是每个人都非常熟悉显微镜,我们需要一个使用方便的系统,事实证明确实如此。”“我们有很多学生在撰写医学论文。他们很快就可以独立使用这台设备分析样品,这种情况前所未有。”当小组中两位博士后研究员在照顾许多学生时,这点也非常重要。在教学和研究过程中,新引入学生的时间可能是有限的,因此,用户友好的系统意味着如果发生某些情况,管理者将位于后台操作,而学生可以自己取得良好的成果。
Baltrusch教授的团队依靠该系统研究糖尿病的方方面面,不仅在分子水平2,而且还研究了与受影响细胞器和细胞相关疾病的更多方面。她介绍了两个有趣的项目:了解线粒体突变在糖尿病中的作用,以及量化高血糖引起的眼内神经元网络损伤。
更新教科书:糖尿病线粒体网络
随着对生物系统过程的了解,曾经被认为是静态组成部分的其实是高度互连的网络,这一认识也越来越明确。线粒体也是如此,Baltrusch教授解释说:“细胞内线粒体的教科书插图通常显示分离的细胞器,每个细胞可能有10-20个细胞器,但实际上并非如此。这是一个正在经历融合与裂变连续过程的动态网络,并且始终在变化。”
有趣的是,已经观察到2型糖尿病与线粒体突变增加之间的相关性。携带线粒体突变和野生型核的塑形小鼠模型非常适合用于理解这种关系。3
“我们想知道当这种突变随着时间积累时会发生什么。” Baltrusch教授说。“线粒体的网络结构或功能是否会改变?研究带有这种突变的小鼠,我们可以看到与野生株相比发生了什么。”
建立糖尿病疾病模型
与Markus Tiedge教授的研究小组*合作,罗斯托克大学对糖尿病的关注也成为针对衰老和疾病的更大规模研究的一部分。在这种情况下,开发糖尿病小鼠模型非常重要,就像Baltrusch教授对于蠕虫最新研究成果的解释:“这很容易-寿命为30天,如果新品系能够存活33天,您可能会得出结论,它的寿命更长,但是将其转移给人类却很困难。”在研究糖尿病中线粒体突变和神经元损伤中,哺乳动物模型提供了更准确的人类表征。

Janine Leckelt研究员在罗斯托克大学研究该小组的糖尿病小鼠模型
图1显示了使用共聚焦显微镜离体培养和可视化的原代小鼠肝细胞。经过图像处理后,可以对单个线粒体进行区分和定量,以检测任何异常拉长或断裂的线粒体。所捕捉图像的质量一直是这一分析水平的核心问题,奥林巴斯FV10i的受欢迎程度已经在该机构得到证明。“当首次在该项目上使用FV10i时,我们在大学的内部研讨会上展示了我们的一些成果。我们的听众对此留下深刻印象,已经拥有共聚焦显微镜的临近小组中有很多人找到我们,问他们是否也可以使用这台机器。如果你看到我们的预订使用登记,就可以发现全都排满了。甚至是昼夜运行,没有空档。”
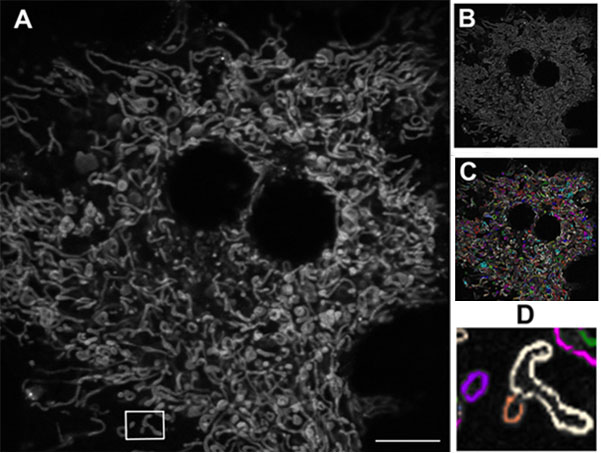
图1:活体小鼠肝细胞中的线粒体网络。
A)原始图像B)进行边缘查找处理(Image J软件,NIH)。C)单个线粒体(Autoquant软件,Media Cybernetics)
D)拉长的线粒体(白色)和破碎的线粒体(紫色和橙色)。使用60X油浸物镜的奥林巴斯 FV10i。比例尺10μm。
在糖尿病中观察到线粒体碎片增多意味着细胞在获取足够能量方面出现问题,并且与骨骼肌的胰岛素耐受性有关。4另一方面,线粒体过度拉长也是问题。有趣的是,研究来自不同网络的图像时,Baltrusch教授的小组发现这很大程度上取决于细胞类型和生理状况。“线粒体网络可以根据需要、可用的能量以及脂肪或碳水化合物的来源进行调整。每个因素都会影响到网络,我们确实学到了很多东西。”
致力于糖尿病性神经病的非侵入性检测
虽然了解糖尿病的潜在机制对于开发新疗法和增进我们对生物系统的了解至关重要,但了解糖尿病对生活质量的影响同样具有价值。
使用奥林巴斯 FV10i的第二个项目致力于开发一种用于及早发现糖尿病性神经病变或神经元损伤的新技术。当高血糖症(血糖水平升高)持续超过五年或更长时间时,生理损害可能会非常严重-神经病变是糖尿病最常见的长期并发症。当血液蛋白糖基化产生所谓的高级糖基化终产物(AGEs)时,就会出现这种情况,后者会结合神经元表面的受体并触发诸如凋亡等破坏性过程。
因此,早期诊断对于疾病的治疗至关重要,然而,由于患者对施加到脚上感觉触发器的口头反应不同,目前的技术无法进行量化。需要一种更定量的技术,并且通过皮肤活检分析神经元网络识别任何丢失的纤维,这不但痛苦,而且伤口愈合对糖尿病患者也是问题。与眼科和视觉科学系**Oliver Stachs教授的小组合作开展的一项研究旨在研究分析眼角膜中的神经元网络。通过使用专门设计的角膜共聚焦显微镜系统,该团队能够观察人类角膜的基底下神经丛。5
这种非侵入性方法适用于糖尿病性神经病变的检测,并且通过更多了解角膜神经结构,该项目致力于将其作为临床定量技术使用。
奥林巴斯 FV10i可与Baltrusch教授小组的糖尿病小鼠模型一起使用,用于定量定量分离离体角膜内的神经密度和长度,从而了解糖尿病性神经病变并指导体内角膜共聚焦显微镜实现最有效的使用。
糖尿病小鼠模型
通过专注一种并非由自身免疫引发的糖尿病,使用化合物链脲佐菌素可特异性破坏胰岛细胞的S细胞。使用胰岛素抗体染色研究样品,并使用共聚焦显微镜观察,图2A显示为固定胰腺切片内完整的胰岛。如图2B所示,其形状与通过胰脏胶原酶消化分离的活体胰岛相当。
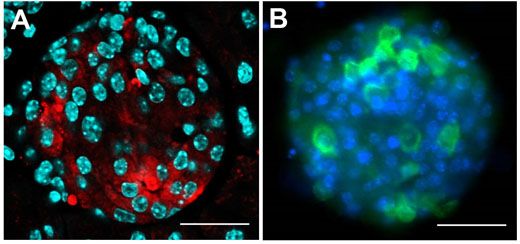
图2:研究小鼠的胰岛细胞。
研究朗格罕氏胰岛中产生胰岛素的β细胞,并通过共聚焦显微镜对其进行观察。A)胰切片染色的胰岛素(红色),核呈蓝绿色。B)培养的胰岛细胞,胰岛素(绿色)和细胞核染成蓝色。使用60X油浸物镜的奥林巴斯 FV10i;比例尺50μm。
查找右神经
使用带有黄色荧光蛋白标记神经纤维的转基因小鼠(thy1-YFP小鼠),可以利用奥林巴斯 FV10i进行角膜神经离体观察。图3显示为基底神经丛较大的基质神经和非常细的神经。但是,角膜的细胞结构较为复杂。6 如图4所示,该神经丛靠近Bowman层,由穿透的A-delta纤维形成,并具有基底下朝向。Baltrusch教授评论说:“基底下神经对损伤非常敏感,可以在糖尿病人和动物中发现这类损伤。”将新技术与旧技术进行比较,并分析了小鼠皮肤标本,由于存在更多的AGEs受体,因此发现角膜神经更容易受到影响。
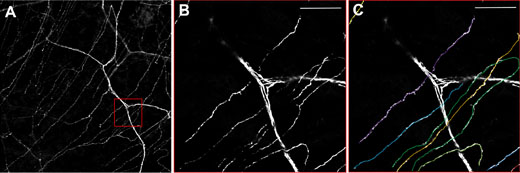
图3:thy1-YFP小鼠角膜中的神经元。
A)概述显示基底神经丛较厚的基质神经和较细的神经。
B)放大红色框,C)定量单个的基底下神经。使用FV10i,60X油浸物镜。比例尺50μm。

图4:小鼠角膜的神经结构。
在使用共聚焦显微镜进行的3D重建中,A delta纤维(黄色)穿透了Bowman层。svve纤维扩散到基底下神经丛(红色)。
她继续解释说:“找到正确的角膜层并分析正确的神经至关重要,但做到非常薄就会很困难。”由于允许选择正确的z位置并有助于3D成像分析,共聚焦显微镜非常适合这一应用。
更大尺寸的图片
这项研究中的一个问题是,若要获得良好的角膜神经元健康状况,需要多少张图片。除神经密度外,神经纤维长度也是神经元健康的指标,而这需要更大的视场。
使用自动图像拼接功能可以让FV10i获得更大的视场。“我们选择FV10i的主要原因之一是为了图像量化和高通量分析,” Baltrusch教授说。“通过在FV10i上进行图像拼接,我们获得了非常不错的概览图。”
图5显示为一夜生成的25个z切片36张图像采集,而四分之一角膜的成像需要三天时间。在这些扩展实验过程中,机器将自动运行,并使用FV10i的自动对焦例程确保扫描视场在多幅图像之间保持对焦状态。这并非共聚焦设备的标准配置,尤其对于紧凑型多合一系统而言并非如此。否则,操作员将需要在机器对焦每幅图像,并且还需要具备拼接高质量图像的经验。为了量化神经纤维密度和单个神经长度,图像拼接可获得更具洞察性的角膜展现。“理想情况下,我们要研究整个角膜,” Baltrusch教授说。尽管FV10i能够获取图像,但这类数据加载需要用于图像分析和定量的专用软件。尽管整个角膜数据将达到160 GB,但是即使从不到四分之一的角膜中所获得的如图5所示拼接图像大约也达到6 GB。
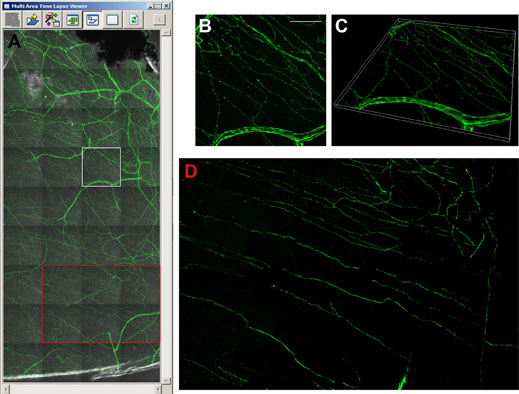
图5:通过图像拼接观察thy1-YFP小鼠角膜。
A)多区域延时查看器显示36个单幅图像,每个图像具有25个z层。标记白色方块的图像显示为3D最大投影(B)和3D体积视图(C)。图像拼接有助于分析基底下角膜神经(A和D中的红色方块)。使用FV10i,60X油浸物镜。比例尺50μm。
未来的研究
除了有助于推动发现神经病变外,这些研究还为Baltrusch教授打开其他研究途径:“我们对哪些区域首先受损很感兴趣,当使用胰岛素治疗小鼠时,首先恢复的是哪里?真正有趣的是,您可以在神经中看到这些点[在图5B中],并且我们知道这些是珠状神经纤维分支,因此对新神经非常重要。”将准确的糖尿病小鼠模型与体内和离体共聚焦显微镜工具相结合,也成为测试用于治疗糖尿病性神经病新化合物的理想平台。
总结
糖尿病是一种与多种因果因素和影响相关的复杂疾病,而使用奥林巴斯FV10i进行共聚焦显微镜检查一直是Baltrusch教授及其研究小组的研究重点。能够实现详细且高通量分析的FV10i在用户友好系统中结合了强大的共聚焦显微镜技术,不但增进了对线粒体网络结构所起作用的理解,还促进了神经病诊断技术的发展。
“即使对于没有显微镜检查经验的人,我们现在也可分析所有组织大约1,000个样品,从而创建整个生物体的糖尿病图像。”让学生和教授都有能力获得高质量的成果是推动学术研究和帮助抗击糖尿病的关键动力。
信息
Simone Baltrusch(博士)教授是罗斯托克大学(德国)医学生物化学和分子生物学研究所的副所长。
合作
* 除了罗斯托克大学医学系的合作研究所之外,医学生物化学和分子生物学研究所所长Markus Tiedge教授的小组
** 罗斯托克大学医学系眼科小组负责人Oliver Stachs教授
参考文献
1. 国际糖尿病联合会(2013年)。IDF糖尿病图集第六版。
www.idf.org/sites/default/files/EN_6E_Atlas_Full_0.pdf
2.Hofmeister-Brix A等人。(2013)Midnolin泛素样结构域作为新的葡萄糖激酶相互作用参与者的鉴定。JBC 288(50):35824-39。
3.Yu X.等人。(2009).使用小鼠塑形菌株剖析mtDNA变异对复杂性状的影响。
Genome Res.19(1):159-65。
4.Jheng H.F.等人。(2012).线粒体分裂导致骨骼肌线粒体功能障碍和胰岛素耐受性。Mol.Cell Biol.32(2):309-19.
5.Zhivov A等人。(2013)无论是否患有视网膜病的健康志愿者和糖尿病患者基底下神经丛的成像和量化。PLoS ONE 8(1): e52157. doi:10.1371/journal.pone.0052157
6.Guthoff R.F等人。(2005)人角膜的上皮神经。Cornea 24(5):608-613
适于这类应用的产品
Maximum Compare Limit of 5 Items
Please adjust your selection to be no more than 5 items to compare at once
对不起,此内容在您的国家不适用。