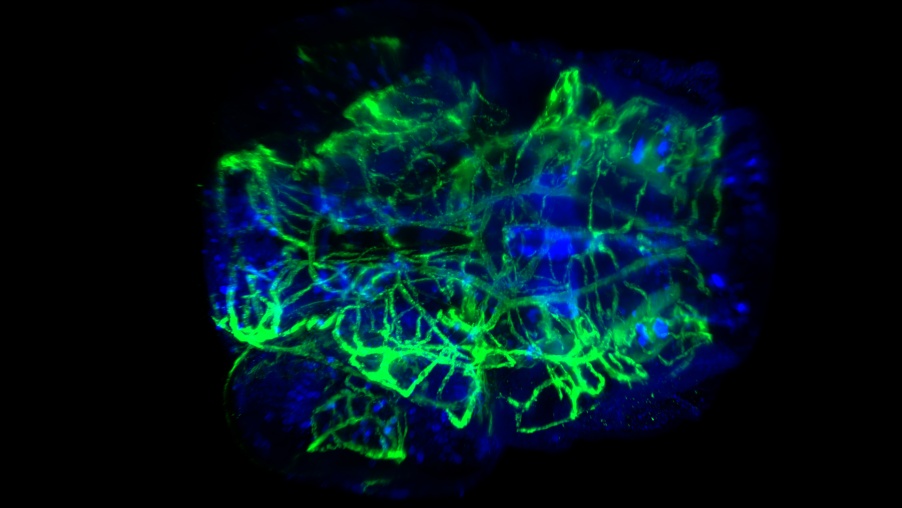
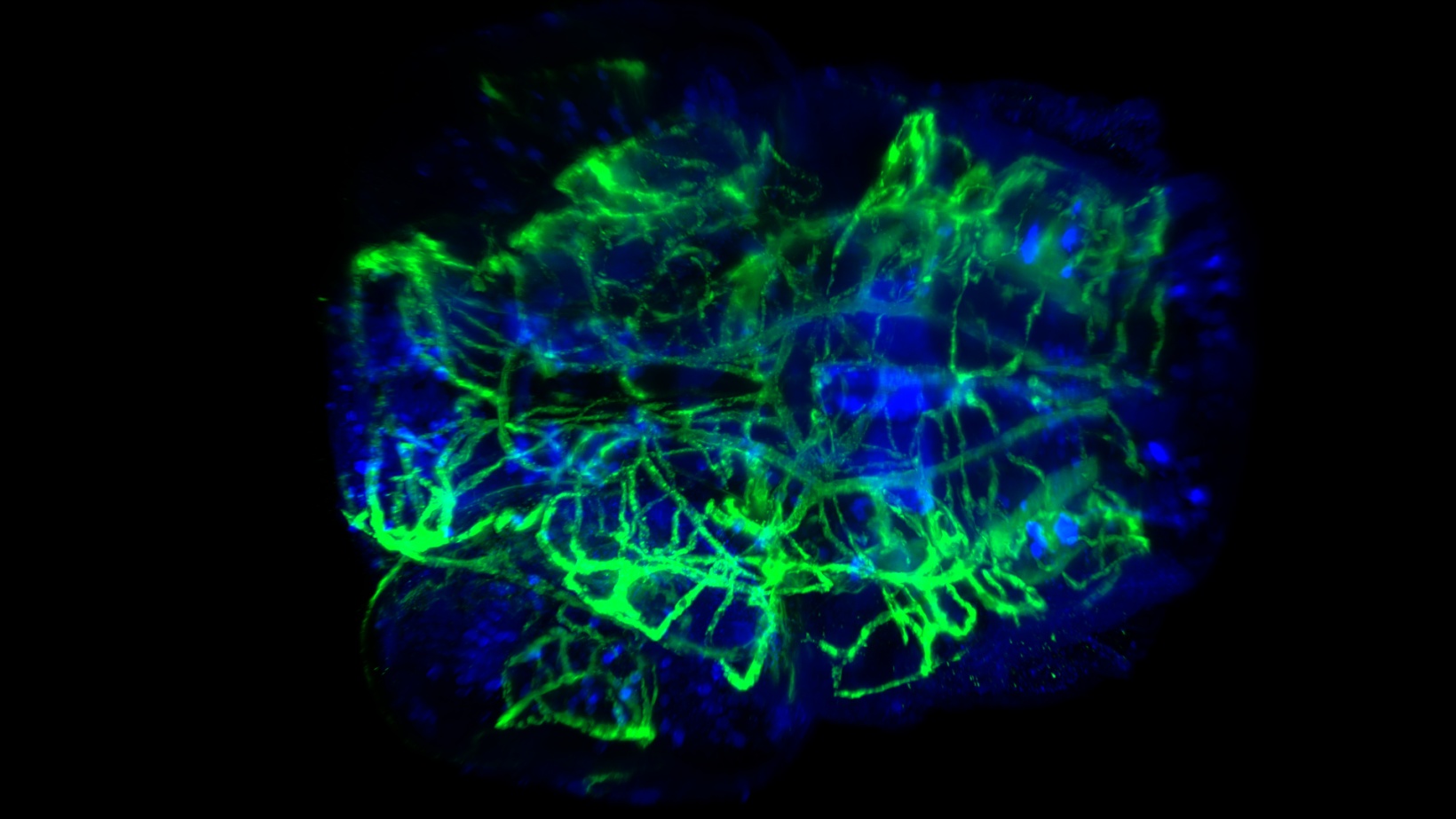
透明化斑马鱼幼虫头部血管和神经。CUBIC-2透明化方法,0.5 NA, 20X物镜采集。图片由法国Tefor Facility的P. Affaticati和A. Jenett提供。
我们生活在一个不断变化的三维世界中。然而在显微镜下,以3D方式观察快速活体过程的成像速度仍然是一个巨大挑战。与其他光学显微成像技术相比,荧光显微成像可以实现较高的特异性和对比度,但仍然存在信噪比和光毒性的限制。
共聚焦显微成像等传统方法可以利用共焦的针孔消除非焦面光的干扰,这一过程被称为光学切片。尽管这一方法具有更高的信噪比,但样品仍需反复暴露于高强度激发光下,从而增加了光漂白的可能性。
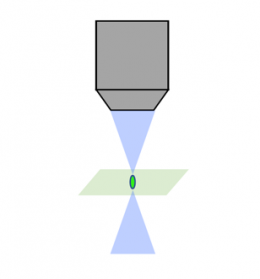 激光扫描共聚焦 | 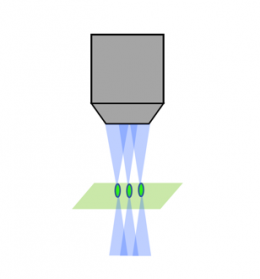 转盘共聚焦 |  光片 |
于是就有了光—光片显微镜的问世
20世纪初,科学家开始寻找改善生物学成像的方法。1902年,随着理查德·西格蒙迪(Richard Zsigmondy)和亨利·西登托普(Henry Siedentopf)开发出一种被称为“Ultramicroscope”(Heddleston&Chew,2016; Adams等,2016)的光学仪器,由此出现了光片技术。这款早期光片显微镜通过分离照明和检测光路突破了光学显微镜传统架构,创造出第一台垂直光片显微镜。
差不多100年后,Voie等人公布了第一张使用垂直平面结构光路对豚鼠耳蜗进行光学切片(Heddleston&Chew,2016; Adams等,2016)的光片荧光显微镜(LSFM)图像。最近,市场上已经出现了对细菌、果蝇、斑马鱼和各种其他组织成像的光片荧光显微镜衍生型号。
让光片荧光显微镜走进更多实验室
现代光片荧光显微镜系统,也称为选择性平面照明显微镜(SPIM),尽管使用圆柱透镜产生用于光学切片的薄照明光片,但也采用了像其前身一样的垂直光路结构。这种薄光片只激发样品在成像物镜焦平面内的一个小范围区域。与传统的共聚焦技术相比,光片荧光显微镜与高速sCMOS相机相结合,可实现更大的采样深度、更高的信噪比和更快的成像速度,从而降低了光毒性。
如今,光片荧光成像已被视为研究整体器官或活体标本的重要显微镜技术。但是,其在科学界的发展仍然受到适用样品有限以及不能有效整合到已有光学系统的限制。近年来,商品化光片荧光显微镜的功能不断增加,日益满足生物领域研究人员的需求。但是,并非所有系统都一模一样,考虑不同功能以满足不同需求非常重要。
比较光片荧光显微镜系统时,需要注意4个方面
在确定哪种光片荧光系统最适合您时,需要考虑几个重要功能。
- 首先是样品制备:
与传统显微成像不同,传统的显微成像通常将较大的固定样本切开并封装在载玻片上,使用光片显微镜成像的样本往往需要进行完整成像,因此必须进行光学透明化,让其变得透明。各种组织的透明化方案有很多种,许多透明化溶液也可购买获得。关于几种常用组织透明化方法,我推荐阅读Pablo Ariel的“A beginner’s guide to tissue clearing”(Int J Biochem Cell Biol.2017年3月84日:35-39)。 - 光学结构:
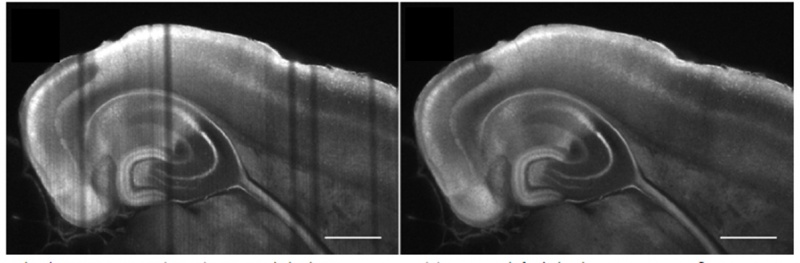
照明和检测光路会显著影响样本的荧光性质和能够检测的样品大小,以及图像质量。例如,条纹伪影是由发射光折射出样品内不透明结构所导致的。为了克服这一问题,已经开发出很多光学系统以适用各种尺寸的活体或透明化样品的成像。多向SPIM(mSPIM)就是其中一种,该系统通过调校多个照明光路来照亮样本并解决条纹伪影问题。尽管mSPIM系统对于特定应用表现良好,但其在灵活性、模块化和实际使用方面均存在局限性,因此在选择最适合您研究的系统时应予以考虑。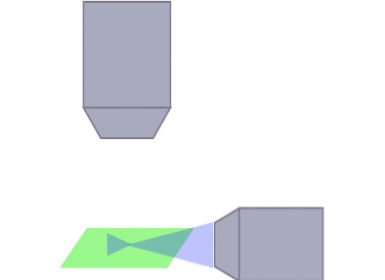
SPIM
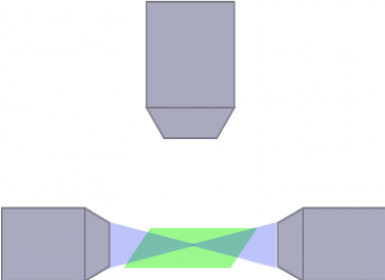
mSPIM
(Schwarz等人,PLoS One,2015年)
- 样品灵活性:
光片荧光显微镜是一个快速发展的领域,每年都会有新的系统推向市场,但由于设计各不相同,其适用的样品类型也存在很大差异。某些系统只能对较小的样本(如肿瘤细胞球)成像,而其他系统则只能对较大的组织成像。其也可能仅限于对固定或活体标本进行成像。尽管这种样品特异性对于专注于一种样品类型的单用户而言可能是理想选择,但却不适于整个研究部门的设备共享或扩展研究范围。考虑您即将采购的光片荧光显微镜系统将要处理的所有可能样本类型是很重要的。最近,更为灵活的光片荧光显微镜系统已经被设计出来,以满足不同样本成像的需要。比如, Alpha3光片荧光显微镜就可以容纳从单个细胞到整个小鼠大脑(包括活生物体)的各种样品。 * - 数据管理:
最后,而且可能最重要的就是数据管理。单次实验达到100GB甚至TB级数据的情况并非鲜见。所以强烈建议您与所在单位的IT部门合作,为您的数据需求制定计划。注意,您可能需要购买单独的分析软件包才能够渲染和分析如此大的数据集。
相关内容
并非在所有地区均可提供*Alpha3系统。请联系您当地的奥林巴斯销售代表了解更多信息。