CM20を用いたヒトiPS細胞株間の比較解析 第二弾:iPS細胞間で見られる肝臓オルガノイドへの分化誘導効率のバラつきについて
はじめに
iPS細胞は、細胞の分化や臓器形成などの発生学に関する基礎研究から、さまざまな疾患に対する創薬・診断法開発の研究まで、幅広く用いられています。中でも、オルガノイドと呼ばれるミニ組織・ミニ臓器をヒトiPS細胞から創出し、人間の代替システム(アバター)としての立体組織を試験管内で創出する技術が飛躍的に進歩しています。現在までに、国内外において樹立された様々な健常者・患者に由来する多数のiPS細胞株を活用してオルガノイドを作製し、その機能の違いや個体差を評価することによって、疾患のゲノム背景や患者ごとの疾患素因を明らかにしようとする研究が世界中で進められています。しかしながら、ヒトiPS細胞から目的とする臓器のオルガノイドを誘導する過程には概して1ヶ月以上の時間と大きなコストを要するにもかかわらず、一般にiPS細胞株間で分化能や増殖の速さなどの性質にバラつきがあることから、オルガノイド創出の安定性や再現性には依然として大きな課題が存在し、多検体比較に基づくオルガノイド研究を進める上での障壁の一つとなっています。
そこで、未分化な状態で日常的に維持しているiPS細胞の状態を長期的かつ定量的にモニタリングすることで、iPS細胞株間に存在する、未分化状態での性質の差とオルガノイドへの分化誘導効率の差にどのような関係性があるのかを検証することにしました。本アプリケーションノートでは、12種類の異なるドナーに由来するヒトiPS細胞株を用いて、それぞれから肝臓オルガノイドを誘導した際、一定の分化誘導プロトコールに沿って培養を行ったにもかかわらず、特定のiPS細胞株では高頻度に肝臓オルガノイドがうまく形成されないケースに着目し、「iPS細胞株間において、分化誘導工程を開始するよりも以前の未分化状態の性質と、肝臓オルガノイドへの分化誘導効率の関係性をいかに追跡するか」という課題にアプローチしています。
オルガノイド分化工程評価に向けた、CM20によって取得したiPS細胞培養データのへの活用
オリンパスのインキュベーションモニタリングシステムCM20は、培養状況を定量的に計測するだけでなく、計測結果をデータとして蓄積し、過去に取得したデータとも容易に比較できます。iPS細胞のコロニー数や密度のデータをCSVファイルにエクスポートすることもでき、より詳細な比較や分析にも展開することが可能です。
今回の研究では、まず、12種類の異なるドナーに由来するヒトiPS細胞株を同時に維持培養して、CM20でモニターし、各株のコロニー数や密度の経時データをエクスポートしました。次に、それらのiPS細胞を、独自の分化誘導プロトコール(※1,2)に沿って、約1ヶ月かけて肝臓オルガノイドへと分化させ、その形成数を計測するとともに、分化指標として肝臓が分泌するアルブミンの量を測定しました。これらのデータを統合して、分化誘導工程前の状態のiPS細胞の情報と、分化誘導した肝臓オルガノイドの情報をiPS細胞株ごとに比較しました。
培養プロトコールおよびデータの解析の詳細説明
ヒトiPS細胞12株を6ウェルプレート中でフィーダーフリー条件にて維持培養しました。培養開始から約1週間後、剥離液Accutaseを用いて単細胞化し、新しいウェルプレートへ播種しました。Activin AとBMP4を処理することで、未分化なiPS細胞から胚体内胚葉に誘導した後、FGF4とWntアゴニストを処理することで後方前腸スフェロイドを得ました。このスフェロイドを、基底膜成分を含むマトリゲルに包埋することで3次元培養へと移行し、オルガノイド形成初期にレチノイン酸(RA)を一過的に導入することで、最終的に約1ヶ月の工程を経て肝臓オルガノイドを形成しました(図1A)。次に、形成されたオルガノイド数をカウントするとともに、培地中に分泌されたアルブミン量をELISAキットを用いて測定しました。このオルガノイドのデータに加えて、CM20から得たオルガノイド分化誘導以前の未分化な状態のiPS細胞の増殖パラメーターを統合し、各iPS細胞株の維持培養における特性とオルガノイド分化効率の間に相関があるかどうかを解析しました(図1B)。
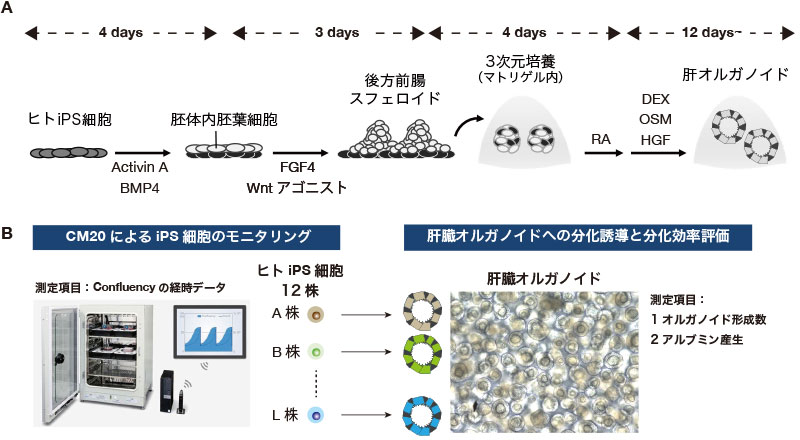
図1 ヒトiPS細胞の維持培養時のモニタリングと、肝臓オルガノイド分化効率の評価
(A) ヒトiPS細胞から肝臓オルガノイドへ分化誘導する培養プロトコールの概要
(B) ヒトiPS細胞の維持培養における特性と肝臓オルガノイド分化効率の株間比較解析の概要
12株のヒトiPS細胞から肝臓オルガノイドへの分化誘導を複数回試みた結果、多くのiPS細胞株からオルガノイドが得られましたが、I株やJ株からはほとんど得られないケースが頻繁にありました(図2A)。また、肝臓オルガノイドからのアルブミン分泌(オルガノイド1個あたりの分泌量を計算)を測定すると、分化誘導の実験回によってバラつきがあるものの、オルガノイドの形成効率が著しく低いI株やJ株から創出されたオルガノイドは、アルブミン分泌も低いことがわかりました(図2B)。オルガノイドの形成効率が高い株(例:C株)の中には、オルガノイド1個あたりのアルブミン分泌量が低いものもありましたが、I株やJ株以外のiPS細胞から創出されたオルガノイドでは、肝細胞特異的なマーカー分子が発現していることが確認できており(データ未掲載)、12株の中ではI株とJ株が肝臓系譜への分化抵抗性の高いiPS細胞株であることが示唆されました。
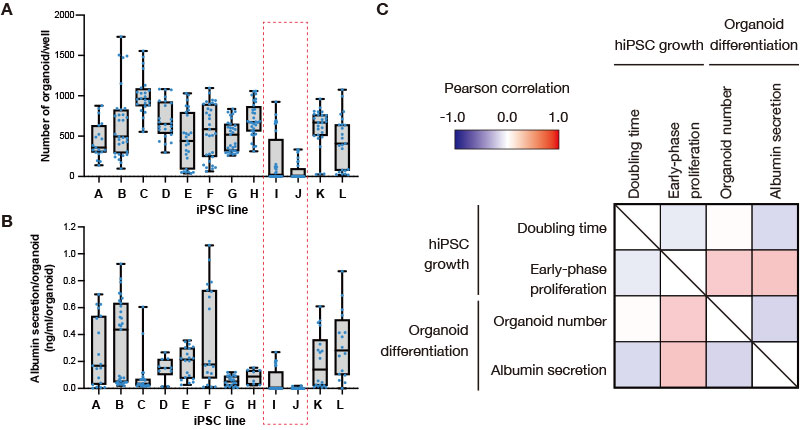
図2 分化誘導工程前のiPS細胞の増殖パラメーターと、形成された肝臓オルガノイドの分化効率の相関解析
(A, B)
複数回実施した分化誘導実験における肝臓オルガノイド形成数(A)とアルブミン分泌量(B)をiPS細胞ごとに箱ひげ図でプロットした。青丸は、複数回の実験で測定したウェル数に対応する。
(C)
分化誘導工程前のiPS細胞の増殖パラメーターとして、倍加時間と増殖初期の増殖効率を、肝臓オルガノイドの分化効率指標として、オルガノイド形成数とアルブミン分泌量を取った場合の各パラメーター間の相関係数を示した。
続いて、分化誘導工程前のiPS細胞の状態が肝臓オルガノイドへの分化効率に影響していたかを調べるため、CM20で取得したiPS細胞の増殖パラメーターと、形成されたオルガノイドの数およびアルブミン分泌量の相関関係を、分化誘導実験回ごとに対応させた状態で解析しました。具体的には、分化誘導工程前のiPS細胞の倍加時間(CM20のconfluencyをもとに算出した値)と増殖初期の増殖効率(武部先生方が独自に定義した式をもとに算出した値)、そして分化誘導後に得られた肝臓オルガノイドの形成数とアルブミン分泌量を実験回ごとでセットにすることにより、異なる実験回の間で生じる誤差を加味した相関解析を行いました(図2C)。その結果、肝臓オルガノイドの形成数やアルブミン分泌量はiPS細胞の倍加時間とほとんど相関が見られない一方、増殖初期の増殖効率のパラメーターとは正の相関があることがわかりました。これは、iPS細胞株間の単純な倍加時間の違いからでは、形成される肝臓オルガノイドの良し悪しは判断できないものの、株間で見られる増殖初期の何らかの違いによって、その後の肝臓オルガノイドの分化効率が左右されている可能性を示しています。
データ比較に基づく考察
CM20は細胞の培養状況が定量的なデータとして記録されるため、オルガノイドへの分化後でも、そこに至るまでの過去の培養状況を振り返って確認することができます。取得した画像やデータは簡単な操作でエクスポートでき、さまざまな分析や解析を可能にするため、新たな知見を得るきっかけにもなります。
今回の研究では、比較を行ったiPS細胞株において、肝臓オルガノイドの形成効率には、維持培養しているiPS細胞の増殖初期における増殖効率が大きな影響を与えている可能性があると明らかになりました。このことから、普段行っているiPS細胞の継代培養において、継代直後からiPS細胞の状態をモニターし、分化誘導に使える状態になっているかを知ることが、肝臓オルガノイドをより安定して、かつより高品質に創出するために重要であると推察できます。さらに、この相関関係をもとに、分化効率のよい細胞株と悪い細胞株がiPS細胞の増殖状態をモニターすることによって予測することも可能であることが示唆されました。
オリンパスは今後も品質管理やデータマネジメントを効率的に行う方法の開発を目指し、CM20を用いた研究を継続していきます。
先生からのコメント
武部貴則教授(左)
| 複数株の異なるドナー由来のiPS細胞をハンドリングし、ドナー間の違いをiPS細胞由来オルガノイドで評価するアプローチにおいて、分化誘導効率がiPS細胞株間でばらついてしまうというトラブルには頻繁に遭遇します。今回チャレンジしたiPS細胞の増殖状態と創出されるオルガノイドの分化効率の相関解析を12株同時に実施する上では、安定した増殖モニタリングと扱いやすいデータ構造のエクスポート機能を持ったCM20の特徴に非常に助けられました。 |
参考文献:
1) Ouchi R, Togo S, Kimura M, Shinozawa T, Koido M, Koike H, Thompson W, Karns RA, Mayhew CN, McGrath PS, McCauley HA, Zhang RR, Lewis K, Hakozaki S, Ferguson A, Saiki N, Yoneyama Y, Takeuchi I, Mabuchi Y, Akazawa C, Yoshikawa HY, Wells JM, Takebe T. Modeling Steatohepatitis in Humans with Pluripotent Stem Cell-Derived Organoids. Cell Metabolism, 30(2):374-384 (2019)
2) 大内梨江、米山鷹介、武部貴則 実験医学別冊 決定版オルガノイド実験スタンダード「多細胞系からなるヒト肝オルガノイドの創出」119-125 (2019)
このアプリケーションノートに関連する製品
Maximum Compare Limit of 5 Items
Please adjust your selection to be no more than 5 items to compare at once
このページはお住まいの地域ではご覧いただくことはできません。
