TruAI™ ディープラーニングテクノロジーを使用したマウス脳切片内のC-Fos陽性ニューロンの定量化
AI(Artificial Inteligence)の進歩—機械学習からディープラーニングへ
AI(Artificial Intelligence)は、研究・技術開発の可能性を大いに広げる先進テクノロジーと考えられてきました。AIは1950年代からその研究が行われ、さまざまな形で使用されています。 広い意味では、AIとは機械が人間の知能を真似できるようにする技術のことです。さらにAIには「機械学習(Machine Learning)」という手法が含まれます。これは、統計学的手法を採用して、機械が明確なプログラミングを使用せずにデータからタスクを学習できるようにするものです。 最も先進的なAIは「ディープラーニング(Deep Learning)」で、数多くのレイヤーを含むニューラルネットワークを構成して、一連の複雑なデータセットからデータ表現の特徴やタスクを直接学習することが可能であり、画像認識の正確性は人間の能力を上回ることもあります。
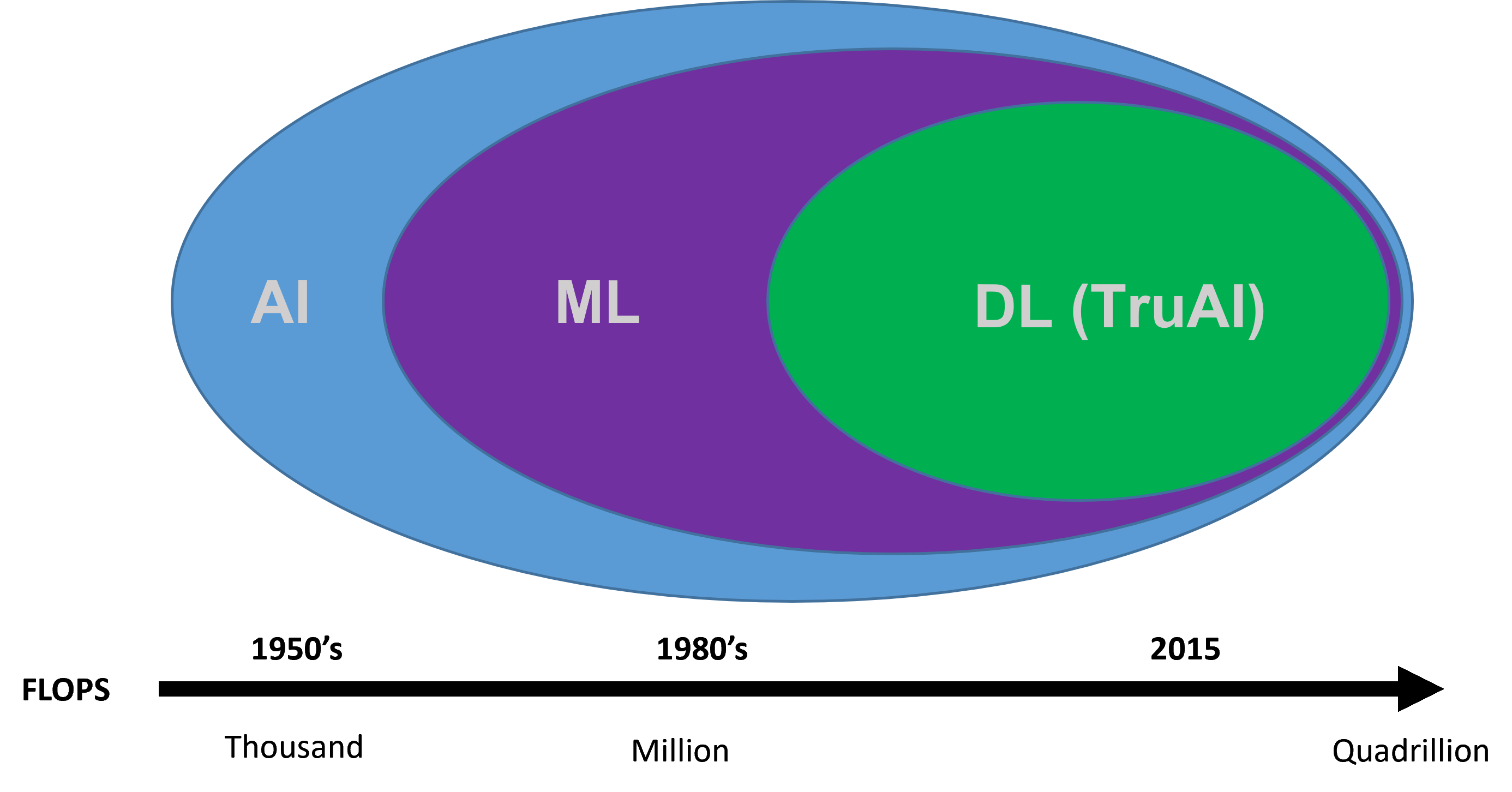
図1: 人工知能開発の年表
顕微鏡観察へのディープラーニングAIの適用
AI、その中でもディープラーニングを顕微鏡画像解析に適用すると、短時間で高精度に、よりロバストな解析を行うことができます。 オリンパスのTruAI テクノロジーのニューラルネットワークは、畳み込みニューラルネットワークを採用しており、顕微鏡画像上の複雑な対象物の難しいセグメンテーションが可能です。さまざまな画像情報の評価や判断といった、人が手動で行った場合にはバイアスがかかりやすい作業に対して、その影響を受けることなく実行することができます。 このアプリケーションノートでは、実際の例として、マウス脳内のc-Fos陽性ニューロンの自動セグメンテーション解析に、TruAIテクノロジーがどのように役立つかについて、従来のAIツールと比較して説明します。
実験の概要:神経新生阻害の系統的評価
この実験では、神経新生阻害を系統的に評価するために、脳の海馬領域(記憶と学習を司る脳の領域)内のc-Fos陽性ニューロンの発現を定量化する必要があります。 C-Fosは、がん原遺伝子の一つで、神経活動のマーカーとして使用されています。従来の輝度/形態によるセグメンテーション法では、画像ごとに背景レベルやターゲットの輝度レベルがまちまちとなりやすく(図2)、手動解析は複雑化し結果から誤検出を除外するのに時間がかかるため、ロバスト画像解析を行うには、あまり効果的でも効率的でもありません。
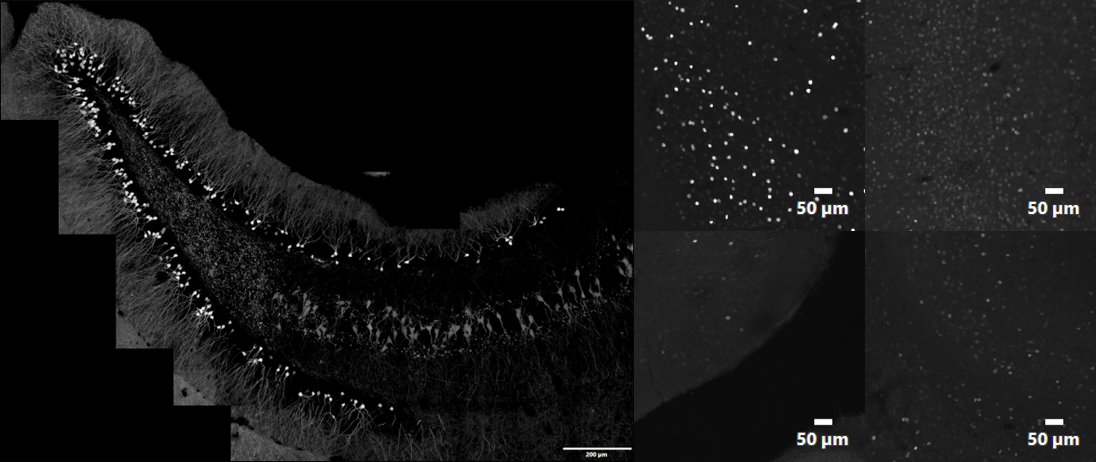
図2: セグメンテーション解析が必要な画像の例: tdTomatoで標識されたC-Fosを発現している、トランスジェニックマウスの海馬領域全体の貼り合わせ画像(左)と、貼り合わせ画像内のc-Fosのシグナル強度と画像背景レベルのバラつき示す個々の画像(右)。 10X SAPOおよび2xズームを使用し、1 AUで取得された1k × 1kのZスタック画像。
C-Fos陽性発現を識別するためのTruAIニューラルネットワークのトレーニング
TruAIのニューラルネットワーク(NN)のトレーニング手順で最初に必要なのは、識別と解析を行うためのグラウンドトゥルース(ground truth)となるトレーニング用画像データセットです。 グラウンドトゥルースは、ユーザーによるハンドラベリングをもとにすることも、cellSensソフトウェアの輝度/形態しきい値設定とセグメンテーション機能を使用して自動生成することもできます。TruAI NNはこれらのトレーニング用画像データセットで反復学習するので、追加で画像入力する必要はありません。 このグラウンドトゥルースによるトレーニングによりTruAI NNが本物(対象)とそうでないもの(対象外)に判断できるように収束させていきます。 実験では、c-Fos発現レベルが異なる8つのデータセットを使用してTruAI NNをトレーニングしました(図3)。 TruAI NNは40,000回の反復からなるロバストトレーニングを行い、それ以降、すべての画像解析に使用するNNを生成しました。 反復トレーニングのプロセス中に、トレーニング用画像セットから選択された画像を検証用として、比較使用しました。
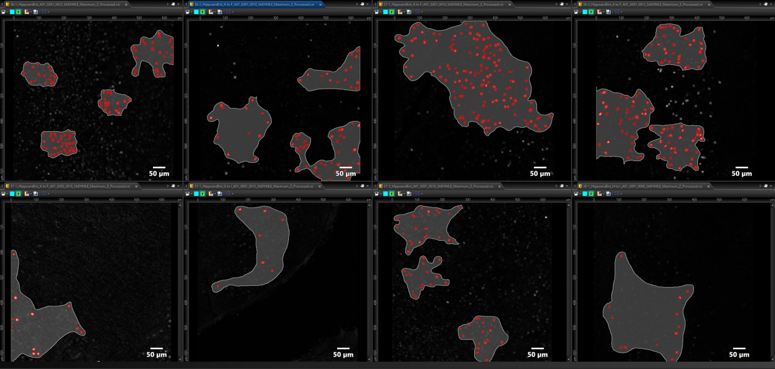
図3: TruAIニューラルネットワーク(NN)生成に使用された8枚のトレーニング用画像データセット: オブジェクト(赤)の発現レベルと背景(灰色)のレベルはそれぞれ異なっている。
バッチ画像解析へのTruAIニューラルネットワークの利用
トレーニングによりTruAI NNを生成したのち、NNを利用して残りの画像データセットのバッチ画像解析を行いました。 図4は、生成されたTruAI NNを使用して生成された確率マップと、その後行われたセグメンテーション解析を示しています。 TruAI NNを使用して、画像データは確立画像に基づいてセグメントテーションされ、さらにcellSensの自動計測アルゴリズムによって、平均輝度、合計輝度、面積に基づくc-Fos陽性細胞の定量解析データが出力されました。 cellSensソフトウェアのマクロマネージャー機能によって、残りのすべてのデータセットがバッチ処理されました。
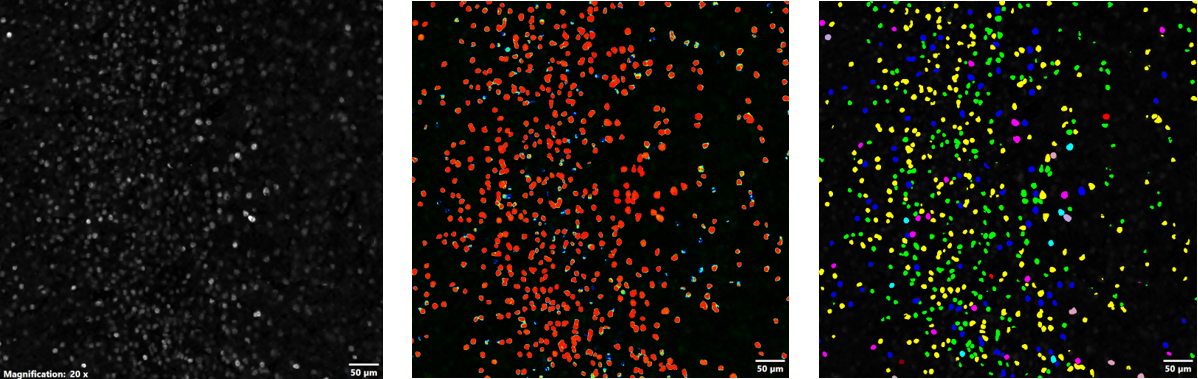
図4: しきい値設定とセグメンテーションにNNを使用: FV3000顕微鏡で取得したc-Fos陽性細胞の画像(左)、NNによって生成されたc-Fos陽性細胞の確率マップ(中央)、確率マップに基づくc-Fos陽性細胞のセグメンテーション(右)。 データは平均輝度、合計輝度、面積に基づいて自動分類されました。
前述のように、画像解析にディープラーニングテクノロジーを使用する利点は、他のAIプログラムよりもロバストなオブジェクト識別が可能である点です。 この実験では、TruAIは画像識別のためのNNを生成するために8つの画像データセットを用意して、40,000回の反復学習をさせました。 ロバストトレーニングの利点は、NNよる画像識別の正確性を増すことであり、理想的ではない画像(例えば、背景が高輝度でターゲット発現が低輝度の場合)であっても、正確なオブジェクトを識別が可能になります。 例えば図5では、1つのトレーニング用画像データセットのみを用いてトレーニングされた、厳密性の劣るネットワークに対して、TruAI NNの性能を比較しました。 発現が高レベルの場合、どちらのアルゴリズムも同程度の細胞数を識別しました。 しかし発現が低レベルの場合、厳密にトレーニングされていないネットワークは、c-Fos陽性細胞の数をほぼ2倍多く見積もり、実験から導き出された結論に大きな影響を及ぼしました。 TruAIディープラーニングテクノロジーは、背景とc-Fosの輝度が変動しても、より正確な結果を出せたため、データから誤検出を除外する手動の修正作業の必要がありませんでした。
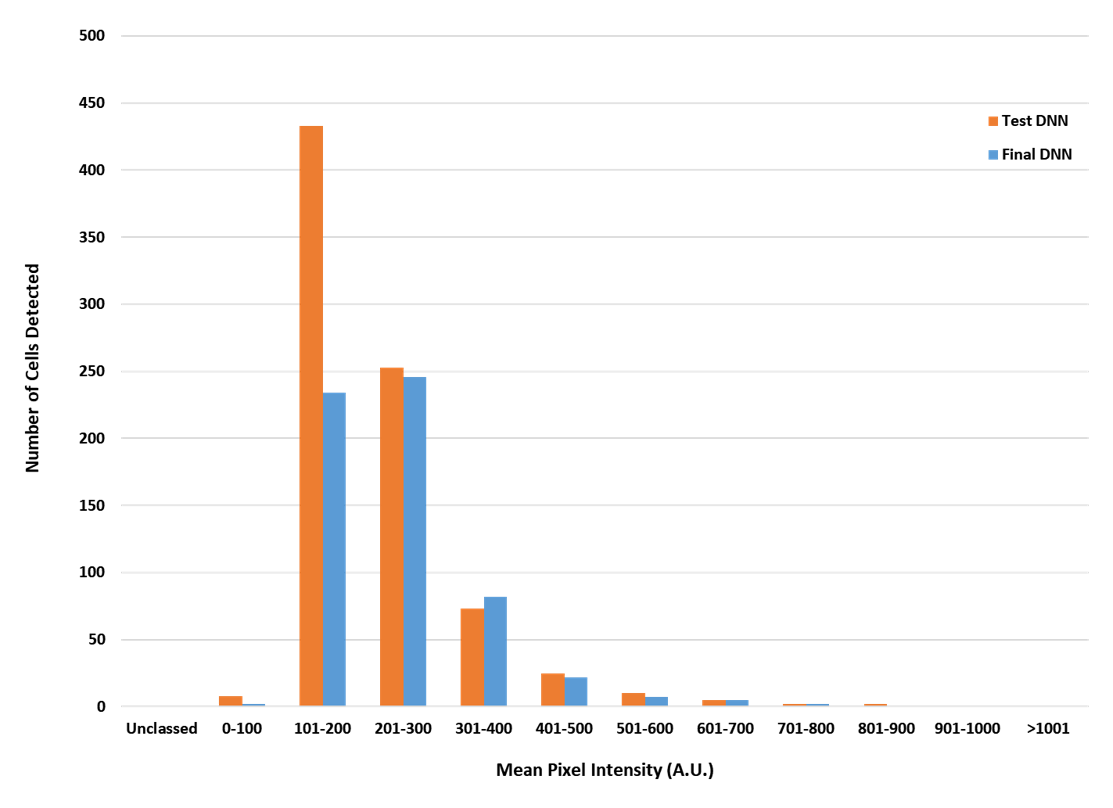
図5: 厳密にトレーニングされていないネットワークとTruAIニューラルネットワークのc-Fos陽性識別率の比較。 オレンジ色の棒は、1つのデータセットを2,000反復させた、厳密にトレーニングされていないネットワークを表し、青色の棒は、8つのデータセットを40,000反復させたTruAI NNの結果を表しています。
研究者Jonathan Epp博士 (カルガリー大学)からのコメント
 | AIの手法が科学研究にとって有益な理由はいくつかありますが、特に重要なのは、画像の定量化時に実験者バイアスをなくすのに役立つという点です。何らかの理由で実験結果に対する先入観があったとしても、AIを使うことで自分自身で顕微鏡画像上で標識された細胞とそうでないものの判断をする必要がないからです。 バイアス以外に、実験者間やラボ内の実験間のばらつきも少なくなり、最終的にはデータの再現性が向上します。 このようなやり方は、近年の科学の現場を悩ませている再現性の問題に対処する手段を講じる上で、大いに役立つと思います。 |
謝辞
このアプリケーションノートは、以下の研究者の協力を得て作成されました。。
Jonathan Epp博士 (カルガリー大学)
このアプリケーションノートに関連する製品
Maximum Compare Limit of 5 Items
Please adjust your selection to be no more than 5 items to compare at once
このページはお住まいの地域ではご覧いただくことはできません。