환자에게서 파생된 종양 오르가노이드의 3D 분석
분자 표적 약물의 항체 결합을 평가하기 위해 NoviSight™ 3D 소프트웨어를 사용하여 환자에게서 파생된 종양 오르가노이드(PDO)의 컨포칼 이미지를 정량적으로 분석하였습니다.
서론
3D 조직 모델은 체내 미세환경과 흡사하기 때문에 신약 개발에 인기가 있습니다. PDO는 원래 환자의 약물 반응을 재현하는 가장 강력한 도구 중
하나입니다. 사실상 최근 연구에서 POD의 표현형 및 유전자형 프로파일링이 원래 환자 종양과의 높은 유사성을 보인다는 것이 밝혀졌습니다. 더 중요한
것은, PDO가 80% 이상의 정확도로 약물 반응성을 예측할 수 있다는 점입니다.
Fukushima 환자에게서 파생된 종양 오르가노이드(F-PDO®), Olympus의 FLUOVIEW® FV3000 컨포칼 레이저 스캐닝 현미경 및 NoviSight 3D 분석 소프트웨어를 사용하여 PDO 형태 및 약제 배포의
새로운 워크플로를 제공합니다.
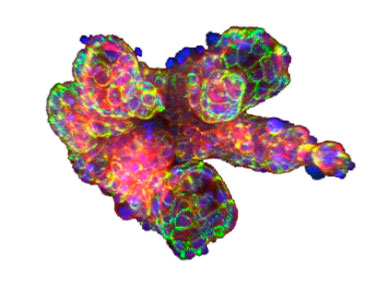
그래프로 된 적요
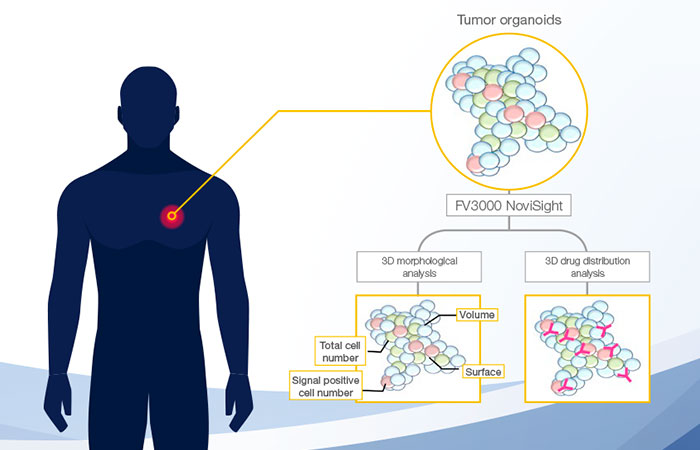
이점
- 3D 구조에 정보를 유지하면서 이미지를 획득하고 PDO를 분석합니다.
- NoviSight 소프트웨어는 3D로 객체를 식별하고 객체를 분류하며 통계 데이터를 제공할 수 있습니다.
방법
세포 준비
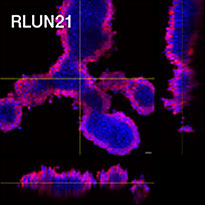
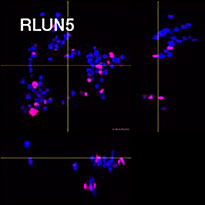
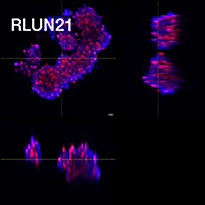
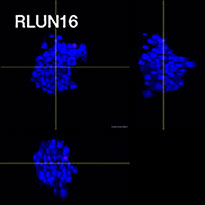
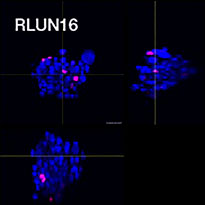
세포를 준비하기 위해 세 가지 유형의 폐 F-PDO(RLUN5, RLUN16, RLUN21)를 사용하였습니다. RLUN5는 선편평상피암 종양에서 생장되고, RLUN16 및 RLUN21은 편평상피암에서 생장되었습니다. RLUN21은 큰 세포군을 형성하고 다른 유형보다 세포질이 더 큰 것이 특징입니다(그림 1).
그런 다음 F-PDO를 원심분리하고 수집하여 하룻밤 동안 4% 파라포름알데히드로 고정시켰습니다. 표피생장인자수용체(EGFR) 억제제인 Erbitux®와 인체 표피생장인자수용체 2(HER2) 억제제인 Herceptin®을 HiLyte™ Fluor 555(Chemical Dojin)로 표지하고 3시간 동안 F-PDO로 배양하였습니다.
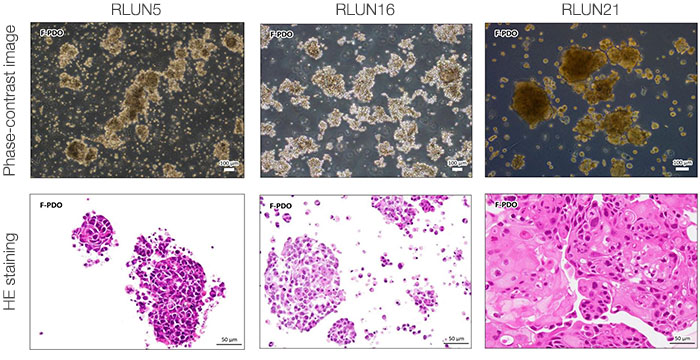
그림 1 F-PDO
면역 염색 및 투명화
Hama 등의 면역 염색 프로토콜을 약간 수정하여 수행하였습니다(그림 2). 고정된 각 F-PDO를 하룻밤 동안 Ki67 항체(Abcam, 16667)로 배양하고 AbScale 용액(0.33M Urea 및 0.2% Triton-X100)으로 희석하였습니다. AbScale로 세척 후 3시간 동안 F-PDO를 2차 항체로 배양하고 AbScale로 희석하였습니다. 1시간 동안 AbScale 헹굼 용액으로 세척 후 4% 파라포름알데히드로 F-PDO를 다시 고정시켰습니다. 그런 다음 인산염완충식염수(PBS) 용액으로 세척하고 DAPI와 함께 투명화 시약 ScaleS4를 사용하여 하룻밤 동안 배양하였습니다. 그런 다음 Olympus의 FV3000 컨포칼 레이저 스캐닝 현미경으로 세정된 F-PDO의 이미지를 획득하였습니다.
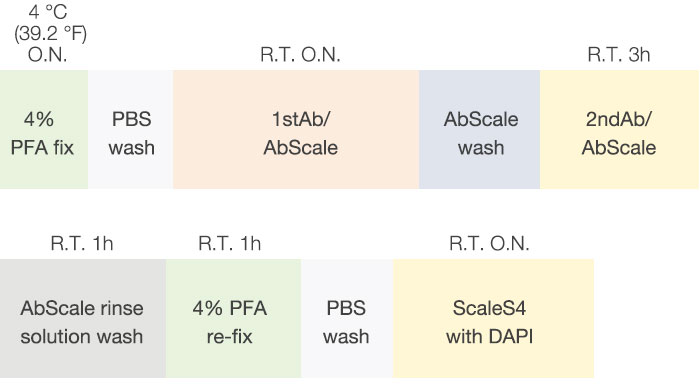
그림 2 F-PDO 면역 염색 및 투명화 계획
이미징 및 분석
3D 분석을 위해 2μm Z 피치로 10× 또는 30× 배율을 사용하여 투명화된 F-PDO의 이미지를 캡처하였습니다.
적절한 Z 피치 설정이 정확한 3D 세포 분석에 중요합니다. 그런 다음 이미지를 NoviSight™ 소프트웨어로 가져와 3D로 복원하였습니다. NoviSight 소프트웨어는 핵 같은 3D
객체를 인식하고 정량적 데이터로 변환할 수 있습니다.
결과
F-PDO 형태의 3D 정량화
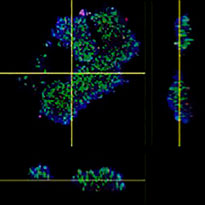
NoviSight 소프트웨어를 통해 여러 Z 평면 이미지를 사용하여 PDO를 정량화할 수 있었습니다. 분석 소프트웨어는 핵을 착색하여 전체 구조를 캡처하고 단세포 인식을 제공하였습니다(그림 3A). 또한 단일 플롯으로 그래프에 각 인식된 객체를 추가하였습니다. 소프트웨어가 각 핵을 객체로 인식하였을 때 높은 Ki67 강도 플롯을 게이팅하여 그래프 및 3D로 Ki67 양성 세포를 추출하였습니다(그림 3B). 이러한 방법을 사용하여 F-PDO의 세포 수, 부피, 세포 밀도 및 Ki67 양성 세포 비율을 정량화하였습니다(그림 3C). RLUN21의 Ki67 양성 비율이 다른 유형보다 더 낮은 것이 밝혀졌습니다. 또한 세포질이 더 크기 때문에 RLUN21의 낮은 세포 밀도가 야기되었을 것입니다.
A | |||
 오리지널 RLUN21 | 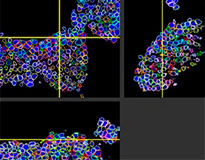 핵 인식 | 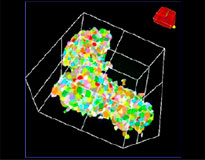 핵 인식 부피 보기 | 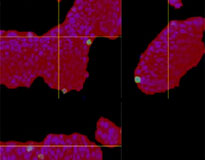 RLUN21 |
B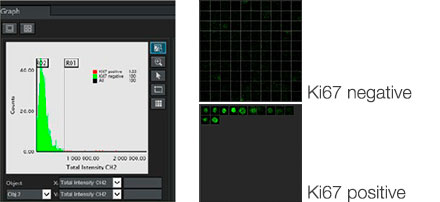 | C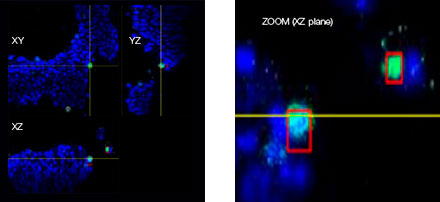 |
D
| RLUN5 | RLUN16 | RLUN21 | |
| 세포 수 | 926 (±719) | 294 (±162) | 2595 (±1480) |
| 부피(화소) | 3.35.E+06 (±3.26.E+06) | 1.08.E+06 (±6.85.E+05) | 1.13.E+07 (±9.12.E+06) |
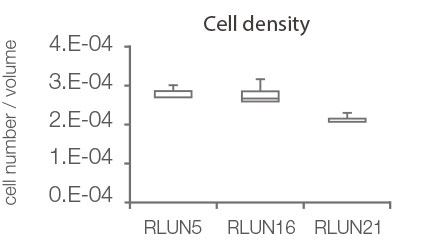 | 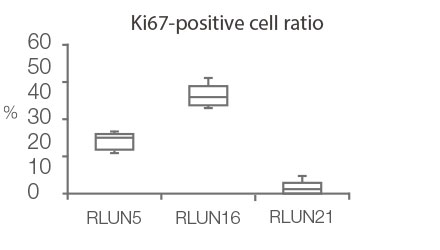 |
| 그림 3 F-PDO 형태의 3D 정량화 |
A. RLUN21, NoviSight 3D 핵 인식(3면 및 부피 보기) 및 NoviSight 구조 인식의 오리지널 3면 보기.
B. Ki67 양성/음성 세포는 Ki67 강도로 분류되었습니다. NoviSight 소프트웨어는 “갤러리 뷰(Gallery view)”에 분류된 세포를 표시할 수 있습니다
C. 분류된 Ki67 양성 세포를 빨간색 원을 사용하여 3D로 표시할 수 있습니다.
D. F-PDO의 정량적 데이터.
3D 약제 배포 분석
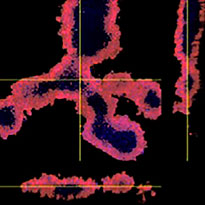
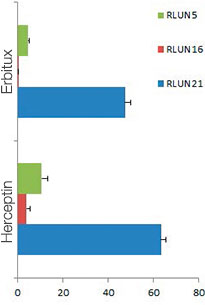
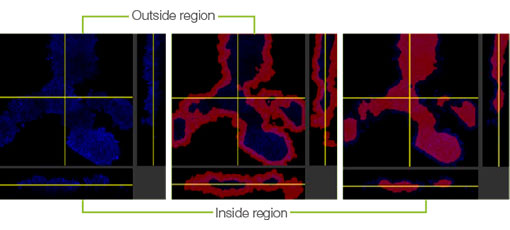
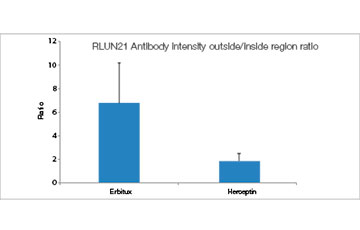
HyLight-555 표지된 Erbitux 또는 Herceptin을 각 F-PDO에 추가하였을 때 Erbitux는 표면에서 RLUN21을 균일하게 결합하였고 Herceptin은 RLUN21을 불규칙적으로 결합하였습니다. NoviSight™ 소프트웨어의 부피 인식 모듈이 항체 약제 양성 부피 비율을 정량화하였습니다(그림 4A). 그런 다음 소프트웨어가 분석 대상 영역을 수정할 수 있기 때문에 NoviSight 소프트웨어를 사용하여 결합 스타일의 차이를 정량화하였습니다. 그렇게 하기 위해 두 가지 대상 영역 즉 특정 비율의 표면에서 감소된 부피 영역과 불특정 폭의 윤곽 부피 영역을 생성하였습니다. 부피 영역 생성 중 항체 약제 강도를 계산하였습니다. Herceptin의 경우와 달리 Erbitux에 감소된 부피와 윤곽 부피 간에 큰 정량적 차이가 눈에 띄었습니다. 즉 Erbitux가 RLUN21 윤곽 영역에 강하게 결합된 반면, Herceptin은 RLUN21에 편향 없이 결합되었습니다. 이 방법으로 항체 약제 배포를 정량적으로 나타낼 수 있었습니다.
A
 |
 |
|
항체 약제
 |
|
 |
|
항체 약제
 |
항체 양성 부피(%)
B
 |  |
| 그림 4 항체 약제 배포의 3D 정량화 |
A. Erbitux 또는 Herceptin이 추가된 F-PDO의 3면 이미지 및 항체 약제 결합의 NoviSight 부피 인식. 그래프는 전체 부피에서 항체 결합 부피를 나타냅니다.
B. NoviSight 영역 수정 모듈. NoviSight은 제한된 영역에서 정량적 데이터를 제공하기 위해 분석 대상 영역을 수정할 수 있습니다.
결론
본 연구에서는 NoviSight 소프트웨어가 Olympus의 FV3000 컨포칼 레이저 스캐닝 현미경으로 캡처된 이미지를 사용하여 형태적으로 및 약학적으로 PDO의 정량 분석을 수행할 수 있음이 밝혀졌습니다. NoviSight 소프트웨어의 고인식 정확도와 FV3000 현미경의 고해상도 이미지를 결합하여 더 신뢰할 수 있는 정량적 결과를 도출할 수 있습니다.
참고문헌
- Vlachogiannis G et al., (2018) Patient-derived organoids model treatment response of metastatic gastrointestinal cancers. Science. 359(6378):920-926. doi: 10.1126/science.aao2774
- Takahashi et al., (2019) An In Vitro System for Evaluating Molecular Targeted Drugs Using Lung Patient-Derived Tumor Organoids. Cells. 8(5), 481. doi:/10.3390
- Tamura H, et al. Evaluation of anticancer agents using patient-derived tumor organoids characteristically similar to source tissues. Oncol Rep.,40, 635-646, 2018
- Hama et al., (2016) Deep Imaging of Cleared Brain by Confocal Laser-Scanning Microscopy. Nature Protocol Exchange. doi:/10.1038 Mayu
저자
Mayu Ogawa(Olympus)
감사의 말
본 연구는 후쿠시마 의과대학 Takagi 교수의 지원을 받았습니다. F-PDO(후쿠시마 환자에게서 파생된 오르가노이드)에 대한 자세한 내용은 다음 웹 사이트를 참조하십시오. https://www.fmu.ac.jp/home/trc/en/contract-research-provision/f-pdo/
이 애플리케이션에 사용되는 제품
Maximum Compare Limit of 5 Items
Please adjust your selection to be no more than 5 items to compare at once
Not Available in Your Country
Sorry, this page is not
available in your country.