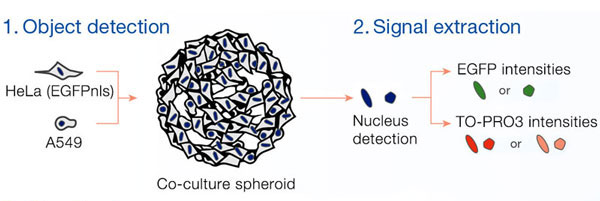
NoviSight™ 소프트웨어를 사용한 공동 배양 암 스페로이드의 3D 분석
세포 집단을 평가하고 각 세포의 약제 감수성을 판단하기 위해 NoviSight 소프트웨어를 사용하여 공동 배양 스페로이드의 컨포칼 이미지를 정량적으로 분석하였습니다.
서론
스페로이드가 암의 복잡한 체외 미세환경을 나타내기 때문에 3D 암 스페로이드를 사용한 약제의 성능 평가가 중요합니다. 이를 통해 연구원들은 종양의 자연 환경과 더욱더 흡사한 매개변수에서 약효를 평가할 수 있습니다.
이러한 애플리케이션에 대한 NoviSight 3D 분석 소프트웨어의 적용성을 평가하기 위해 A549 세포 및 HeLa 세포의 암 스페로이드를 공동 배양하였습니다. 그런 다음 NoviSight 소프트웨어를 사용하여 이들 세포에 대한 약물 처리의 효과를 3D로 분석하였습니다. 본 연구에서는 객체가 포함하는 정보에 따라 객체를 분류하고 약효를 평가하기 위해 각 매개변수를 분석하는 데 NoviSight 소프트웨어를 성공적으로 사용할 수 있음을 증명하였습니다.
![]()
그래프로 된 적요
 | |
 |  |
이점
- 신호를 기준으로 두 가지 세포 유형을 분류할 수 있으며 집단 분석을 수행할 수 있습니다.
- 스페로이드의 중심 및 주변 영역을 분리하여 약효를 공간적으로 분석할 수 있습니다.
방법
세포 준비
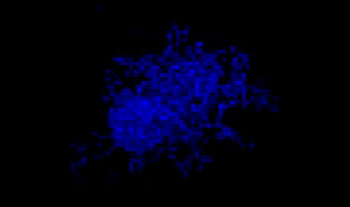
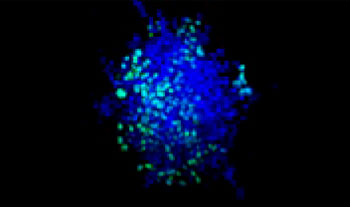
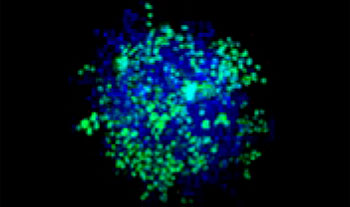
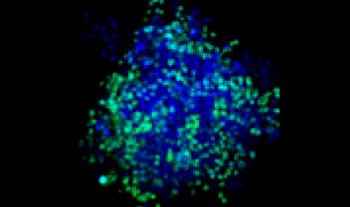
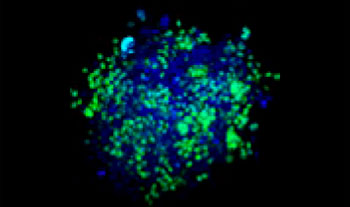
A549 인간 폐 세포와 HeLa 자궁경부 암세포(핵 내 EGFP 발현됨)가 다양한 비율로 혼합되었습니다. HeLa 세포의 비율은 EGFP 신호의 강도에 따라 보정되었습니다(그림 1*1). 세포가 Corning® 384웰 원형 바닥 플레이트(웰당 200개 세포)에 파종되었으며 10% FBS로 DMEM에 3일 동안 배양되었습니다. 플레이트를 부드럽게 원심분리하여 웰의 기포를 제거하였습니다.
A549: HeLa-EGFPnls
100:0
| 75:25
| 50:50
| 25:75
| 0:100
|
그림 1. 준비된 공동 배양 암 스페로이드*1
샘플 준비
샘플은 스페로이드에서 A549 세포와 HeLa 세포의 1:1 비율이 되도록 3.7nM~3.75μM의 농도로 5시간 동안 스타우로스포린(STS)으로 처리되었습니다. 막투과성의 차이를 이용하여 모든 핵들을 10μM의 Hoechst33342(DOJINDO)로 착색하고 죽은 세포의 핵들을 1μM의 TO-PRO3(Thermo Fisher Scientific®)으로 착색하여 세포 생존율을 결정하였습니다. 그런 다음 샘플을 1x PBS로 세 번 세척하고 4°C(39.2°F)로 하룻밤 동안 4% 파라포름알데히드로 고정시켰습니다. 이미징 전에 스페로이드는 실온에서 하룻밤 동안 SCALEVIEW-S4(FUJIFILM Wako) 조직 투명화 시약으로 처리되었습니다.
이미지 및 분석
A 라인 슈퍼 아포크로맷 렌즈 대물렌즈(UPLSAPO30XS)가 있는 FLUOVIEW® FV3000 컨포칼 레이저 스캐닝 현미경을 사용하여 스페로이드의 형광 이미지를 획득하였습니다. 고품질 및 3D 형태를 제공하기 위해 이멀젼 액의 굴절률이 일치하도록 대물렌즈의 보정환을 조정하였습니다. 여러 이미지를 NoviSight™ 3D 세포 분석 소프트웨어로 가져와 3D로 복원하였습니다. NoviSight 소프트웨어는 핵 같은 객체를 인식할 수 있으며 객체에 포함된 다양한 신호를 다양하게 분석할 수 있습니다.
결과
공동 배양 스페로이드의 약제 감수성 이미징
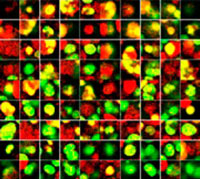
스페로이드를 투명하게 만들고 FV3000 컨포칼 레이저 스캐닝 현미경을 사용한 이미징 수행을 통해 공동 배양된 암 스페로이드의 심도 있는 이미지를 획득할 수 있었습니다. 스타우로스포린 처리는 투여 의존적 방식으로 죽은 세포 수를 증가시켰습니다(그림 2*1). 어느 세포가 죽었는지와 3D 질량으로 있는 죽은 세포의 수를 판단하기 위해 3D 분석이 필요합니다.
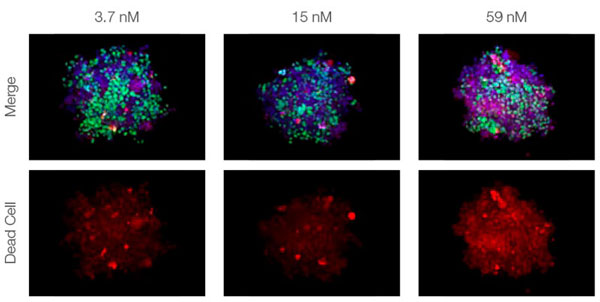
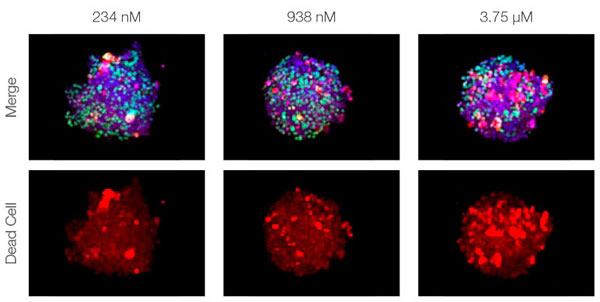
그림 2. 공동 배양 스페로이드의 약물 반응*1
공동 배양 스페로이드의 약제 감수성 분석
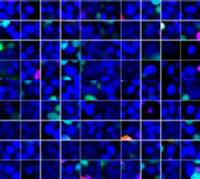
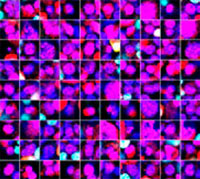
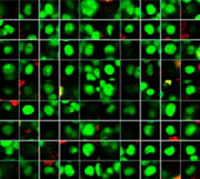
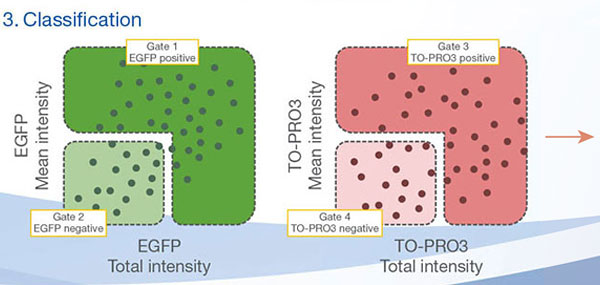
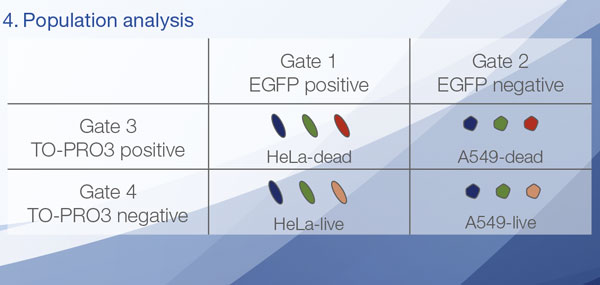
Hoechst33342 신호를 통해 핵들을 인식할 수 있었습니다. 모든 세포는 EGFP 신호의 존재 또는 부재 즉 EGFP 양성(HeLa 세포) 및 EGFP 음성(A549 세포)을 기준으로 두 그룹으로 분류되었습니다. 또한 이들 두 그룹의 세포들은 총 4그룹에 대해 죽은 세포 신호(TO-PRO3, 빨간색)의 존재 또는 부재에 따라 나뉘었습니다(그림 3*1). 살아있는 세포 대 A549 세포 및 HeLa 세포의 총수의 비율을 계산하여 표시하였습니다(그림 4). 그 결과, HeLa 세포가 A549 세포보다 스타우로스포린에 더 민감한 것으로 밝혀졌습니다.
NoviSight™ 소프트웨어를 사용하여 각 공동 배양 암 스페로이드에 포함된 세포 유형을 분류하고 세포 유형별 약물 반응성을 분석할 수 있었습니다.
| 갤러리 |
|
|
|
|
| Hoechst | + | + | +*2 | +*2 |
| EGFP | - | - | + | + |
| TO-PRO-3 | - | + | - | + |
그림 3. NoviSight 소프트웨어는 신호를 기준으로 세포를 4그룹으로 분류할 수 있습니다*1
*2 우측 두 갤러리에는 Hoechst 신호가 나타나지 않습니다
스타우로스포린 농도
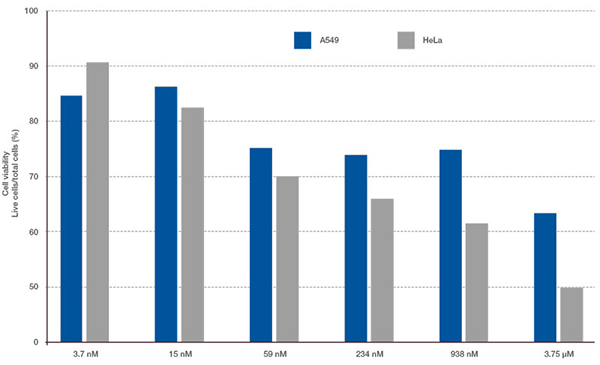
그림 4. A549 세포와 HeLa 세포 간 약물 반응성의 차이
공간 분석 전략
더 복잡한 공간 분석을 수행할 수 있도록 이미지를 3D로 캡처합니다. 이를 통해 암 같은 이종 조직의 세포 거동을 분석할 수 있습니다. NoviSight™ 소프트웨어는 분석 대상 영역을 설정할 수 있습니다. 각 스페로이드의 중심부 및 주변부와 생성된 8개 그룹을 모두 분석하도록 소프트웨어를 설정하였습니다(그림 5). 그런 다음 이들 영역 내에서 집단 분석을 수행하였습니다(그림 6). 이 방법을 통해 공동 배양 암 스페로이드에서 약효의 공간 분석을 수행할 수 있습니다.
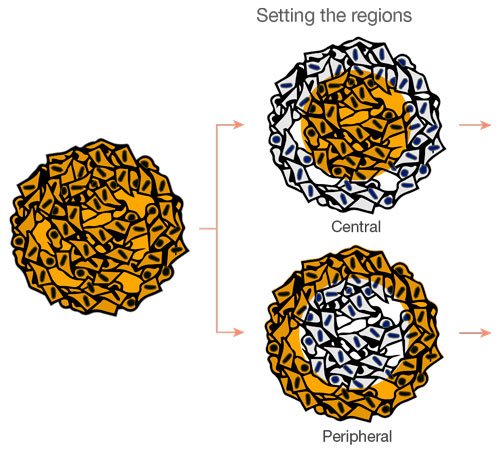 |  |
그림 5. 공간 분석의 개략도
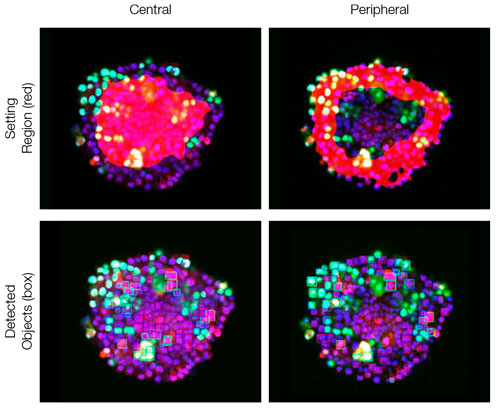
그림 6. NoviSight 소프트웨어는 중심부와 주변부를 분류할 수 있습니다
약효의 공간 분석
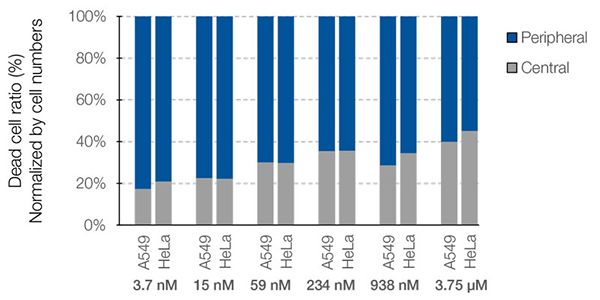
NoviSight™ 소프트웨어는 죽은 세포의 수를 계산할 수 있을 뿐 아니라 약물의 공간 효과도 분석할 수 있습니다. 이 기능을 입증하기 위해 공동 배양 스페로이드에서 각 죽은 세포의 공간 분석을 수행하였습니다. 중심 및 주변 영역 내 세포 수 대 각 죽은 세포의 비율을 계산하였습니다(그림 7). 이 경우에 이들 영역 간 약효의 차이는 없었습니다. 중심부와 주변부 내 죽은 세포의 수가 투여 의존적 방식으로 증가하였습니다.
스타우로스포린 농도
그림 7. 중심 및 주변 영역 간 약물 반응성의 차이
결론
NoviSight 소프트웨어 및 FLUOVIEW® FV3000 컨포칼 레이저 스캐닝 현미경을 사용하여 공동 배양 스페로이드에 포함된 세포 유형을 분류하고 세포 유형별 약물 반응성을 분석할 수 있었습니다. 공동 배양의 결합을 변경하여 다양한 암의 미세환경을 성공적으로 재현할 수 있으며 항암제의 효과를 평가할 수 있습니다.
저자
Hiroya Ishihara, 생물학적 평가 기술 2, 연구개발
*1 비록 헬라 세포가 의료 연구에서 가장 중요한 세포주가 되었다고 해도, 과학에 대한 Henrietta Lacks의 공헌이 동의를 받지 않은 것이었다는 것을 인정해야만 합니다. 이로 인해 면역학, 전염병, 암에 대한 중요한 발견이 이루어졌지만 사생활, 윤리, 의학적 동의에 대한 중요한 논의도 촉발되었습니다.
Henrietta Lacks의 삶과 현대 의학에 대한 그녀의 공헌을 알아보려면 여기를 클릭하세요.
http://henriettalacksfoundation.org/
이 애플리케이션에 사용되는 제품
Maximum Compare Limit of 5 Items
Please adjust your selection to be no more than 5 items to compare at once
Not Available in Your Country
Sorry, this page is not
available in your country.