- Introduction
- Configuration de l’imagerie
- TruSpectral
- Macro to Micro Imaging
- Configuration pour l’électrophysiologie
- Frame Design
- High Speed Imaging
- Interface for Electrophysiology
- Bouton de préinscription
Introduction
Découvrez nos systèmes FLUOVIEW droits et leurs possibilités infinies !
Olympus a développé deux versions du microscope droit FLUOVIEW FV3000 pour les expériences in vitro et in vivo. Vous pouvez désormais profiter de la vitesse et de la flexibilité du microscope confocal à balayage laser le plus avancé d’Olympus dans une configuration droite.
Configuration de l’imagerie
Configuration de l’imagerie
 | La stabilité pour une imagerie encore plus fiableLa platine fixée au statif du BX63LF améliore la stabilité et assure une imagerie de précision. En plus de cette stabilité, le déplacement motorisé de la tourelle sur l’axe Z est très précis, ce qui contribue à une capture fiable des images d’empilement en Z. Facile à utiliserLe microscope est équipé d’une tourelle porte-objectifs motorisée et d’un condenseur universel motorisé, ce qui permet de choisir automatiquement l’élément optique correspondant à l’objectif. Vous pouvez fixer jusqu’à sept objectifs sur la tourelle de grossissement allant de 1,25X à 150X. Ces caractéristiques permettent un gain de temps et améliorent les performances d’observation en continu avec des grossissements de faibles à élevés. |
TruSpectral
Imagerie spectrale multicanale avec la détection TruSpectral
Doté de la technologie TruSpectral sur tous les détecteurs, le système FV3000 allie une sensibilité élevée à une grande précision pour vous apporter d’excellentes capacités d’imagerie spectrale. *US8530824B/JP5541972B/EP2395380A *Vidéo : image 3D d’un ganglion ciliaire de poussin nettoyé à l’aide d’un réactif de nettoyage de tissu. Données d’images fournies avec l’aimable autorisation du Dr Ryo Egawa. Tohoku University Graduate School of Life Science. |
Macro to Micro Imaging
Imagerie macro à micro
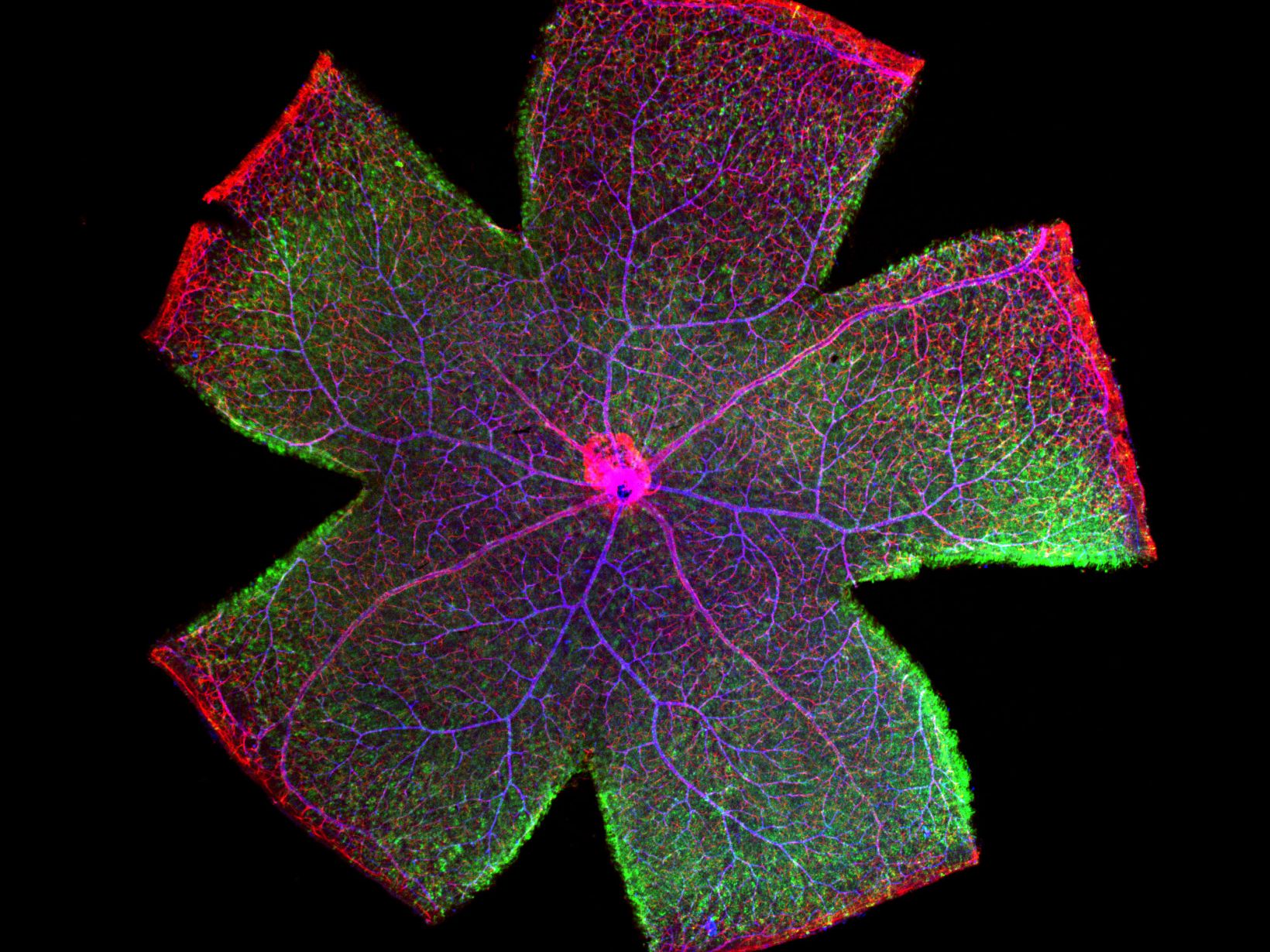
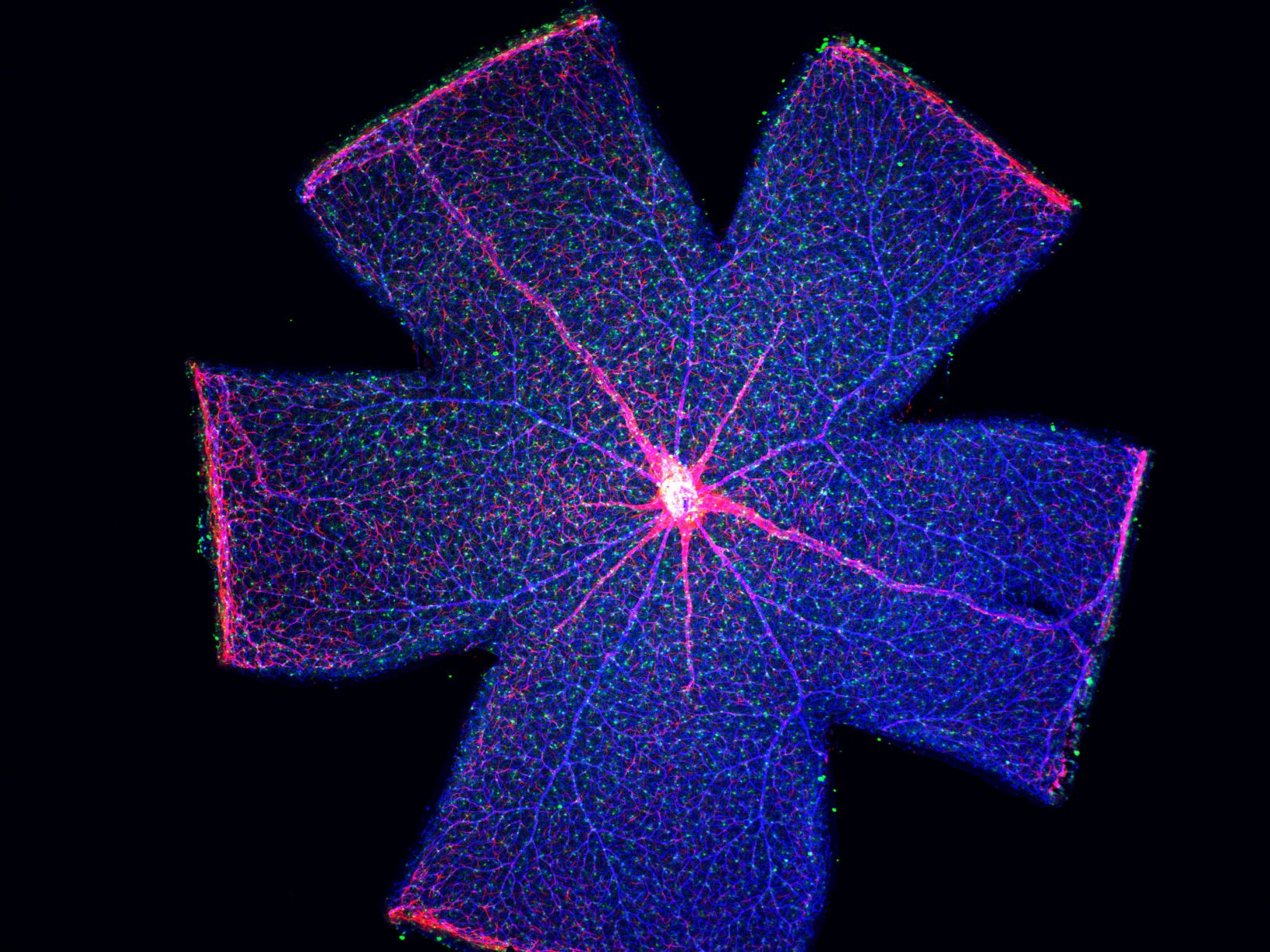
Le FV3000 présente une trajectoire optique macro à micro optimisée pour capturer des images allant de 1,25X à 150X. Trouvez rapidement des régions d’intérêt avec des aperçus à faible grossissement, puis basculez sur des grossissements plus élevés pour obtenir des images de haute résolution. L’algorithme d’assemblage robuste du système permet d’obtenir des images macro de haute résolution qui montrent les échantillons dans leur contexte. *Image : rétine de souris Image d’aperçu en une prise capturée par le PLAPON2X. Données d’images fournies avec l’aimable autorisation du Dr Yoshiaki Kubota, The Laboratory of Vascular Biology Center for Integrated Medical Research, School of Medicine, Keio University. |
Configuration pour l’électrophysiologie
Configuration pour l’électrophysiologie
 | Deux tourelles porte-objectifs pour l’électrophysiologiePour les applications d’électrophysiologie, vous pouvez choisir entre une tourelle porte-objectifs pivotante ou coulissante. La tourelle porte-objectifs pivotante est compacte et pivote de l’avant vers l’arrière, permettant ainsi aux utilisateurs de changer les objectifs en immersion dans l’eau sans interférer avec les électrodes. La tourelle porte-objectifs coulissante dispose d’un objectif d’un diamètre de 25 mm et d’une distance parfocale de 75 mm, et d’un second objectif muni de parties filetées de diamètre normal (RMS). Cette tourelle porte-objectifs glisse horizontalement, ce qui facilite le changement d’objectif et libère plus d’espace de travail. Les deux tourelles porte-objectifs sont codées, ce qui permet au logiciel d’indiquer l’objectif qui est en cours d’utilisation. Compensation Senarmont pour l’observation DIC (contraste interférentiel différentiel)Pour réduire le risque de collisions entre la platine, l’échantillon, les manipulateurs ou la tourelle porte-objectifs lors de l’utilisation de la fonction DIC compensé Sernamont, le polariseur rotatif a été placé sur la base du statif du microscope. L’emplacement du polariseur est également bénéfique pour l’IR-DIC afin d’observer des cellules profondes à l’intérieur d’une tranche d’encéphale. |
Frame Design
Un cadre adapté à l’électrophysiologie
 | Cette configuration libère l’espace de travail pour accueillir le matériel d’électrophysiologie autour de l’objectif. Vous pouvez l’optimiser davantage en diminuant la hauteur de la platine pour réaliser vos expériences sur des échantillons de grande taille. |
High Speed Imaging
Imagerie à haute vitesse
Obtenez des images confocales vidéo à l’aide du scanner à résonance du système, sans compromettre le champ d’observation.Plage de vitesses allant de 300 images par seconde à 512 x 512 jusqu’à 438 images par seconde à 512 x 32. Ces vitesses font du FV3000 un outil particulièrement adapté à l’imagerie en temps réel d’évènements physiologiques, comme le flux d’ions calcium. *Vidéo : images avec rapport IMD de l’oscillation spontanée de Ca2+ dans une cellule myocardique battante de rat s’exprimant sous forme de caméléon jaune. Données d’images fournies avec l’aimable autorisation du Dr Yusuke Niino et du Dr Atsushi Miyawaki, Cell Function Dynamics, Brain Science Institute of RIKEN. |
Interface for Electrophysiology
Interface pour l’électrophysiologie
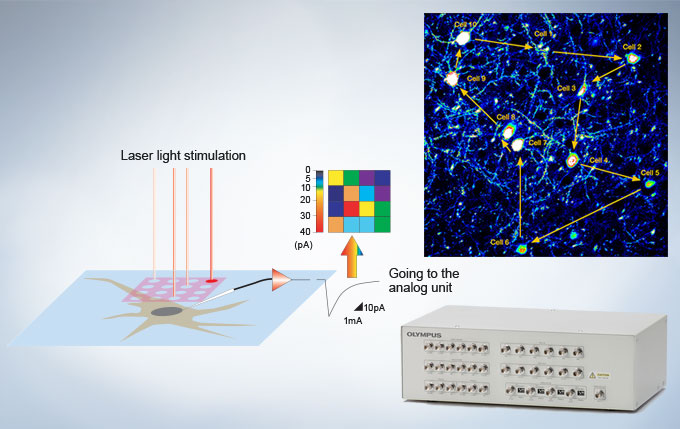 | Un boîtier d’interface de signal I/O de déclenchement est disponible pour synchroniser une imagerie confocale avec un équipement d’électrophysiologie. Le boîtier d’interface convertit des signaux de tension électrique en images, qui peuvent être traitées de la même manière que des images en fluorescence afin d’obtenir des images synchronisées avec la photostimulation du scanner confocal. |
Bouton de préinscription
Not Available in Your Country
Sorry, this page is not
available in your country.
.jpg?rev=EE19)